Поведение - водород
Cтраница 2
После рассмотрения некоторых правил поведения гидридного водорода в комплексах борина мы можем познакомиться с химическим поведением комплексов, в которых атом основания имеет более или менее активный протон. Это обстоятельство может вызвать два вида неустойчивости: простую диссоциацию на диборан и основание или взаимодействие протона с атомом водорода, связанным с бором, с образованием молекулярного водорода и замещенных производных группы борина. Примеры, которые здесь приводятся, показывают существенные различия в обоих видах неустойчивости. [16]
Экспериментальные данные показывают, что поведение водорода при комплексонном режиме зависит от двух факторов: 1) дозы комплексона; 2) температуры ( энтальпии) среды. Дозой комплексона определяется уровень концентрации водорода в тракте котла. [17]
Рассмотрим с этой точки зрения поведение водорода и его влияние на свойства стали при комнатной температуре. [18]
При дозировании комплексен а характер поведения водорода по тракту остается прежним, но абсолютные значения начиная с температуры 300 - 330 С возрастают. [19]
Изложенные результаты наших опытов по поведению водорода в стали имеют непосредственное отношение не только к определению водорода методами хранения, вакуум-нагрева и вакуум-плавления, но и любыми другими методами. [20]
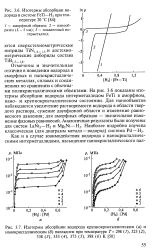 |
Изотермы абсорбции во - 1пр дорода в системе FeTi - Н2 при температуре 20 С.| Изотермы абсорбции водорода крупнокристаллическим ( а и. [21] |
Отмечены и значительные отличия в поведении водорода в аморфных и нанокристалличе-ских металлах, сплавах и соединениях по сравнению с обычными поликристаллическими объектами. На рис. 3.6 показаны изотермы абсорбции водорода интерметаллидом FeTi в аморфном, нано - и крупнокристаллическом состоянии. Для нанообъектов наблюдаются увеличение растворимости водорода в области твердого раствора, сужение двухфазной области и изменение равновесного давления; для аморфных образцов - значительное изменение фазовых равновесий. [22]
По-видимому, электродинамический фактор изнашивания должен влиять на поведение водорода в зоне фрикционного контакта. Этот вопрос требует специального исследования. [23]
По-видимому, с этим связано отличное от малоуглеродистой стали поведение водорода в титанистой стали. Сохраняя при обжиге эмалевого покрытия ферритное строение, титанистая сталь растворяет меньше водорода, а вследствие образования прочных гидридов, гидрокарбидов и гидронитридов титана выделение водорода из стали после затвердевания эмали, нанесенной на поверхность титанистой стали, практически не происходит. [24]
Очевидно, что термическая и термомеханическая обработка материала влияет на поведение водорода в никелевых сплавах. Располагая информацией по вопросам физического металловедения таких сплавов ( см. обзоры [123, 126, 271-277]), можно было бы попытаться подробно описать микроструктурные факторы, определяющие такое поведение. [26]
Анализ результатов расчетов позволяет сделать вывод, что методика Ли-Эдмистера описывает поведение водорода в несколько раз точнее, чем методика Чао-Сидера. По метану и этилену точности воспроизведения фазового поведения по методам Чао-Сидера и Ли-Эдмистера близки друг другу. [27]
С целью выяснения влияния типа цеолита и природы введенного иона на поведение водорода на поверхности цеолитов исследованы реакции дейтероводородного обмена с цеолитом и в молекулах водорода на его поверхности, а также процесс разделения изотопных молекул водорода. При изучении катионных форм металлов было обнаружено, что в температурном интервале от - 196 6 до 220 - 280 - 300 С для цеолитов типа А, X, Y соответственно практически не происходит H-D обмена адсорбированного водорода с водородом гидроксильных групп цеолитного каркаса типа А. Для Х - и У-цеолитов максимальный обмен наблюдали для никелевого, кобальтового и хромового образцов. [28]
Рассмотрим еще одну гипотезу, выдвижению которой предшествовали многочисленные и обстоятельные исследования поведения водорода, главным образом в титановых сплавах. В этих работах, возглавляемых Б.А.Колачевым, постепенно было сделано предположение о том, что главным эффектом, определяющим свойства металла в присутствии растворенного водорода, является транспортировка атомов водорода движущимися дислокациями, в результате чего на границах зерен, межфазных границах и у других препятствий, где накапливаются дислокации, концентрация водорода становится достаточной для резкого ускорения разрушения металла по тем или иным механизмам. Таким образом, в этой гипотезе авторы главную роль отводят не статическому, а динамическому фактору, считая, что общим моментом во всех случаях водородной хрупкости является транспортировка водорода к препятствиям, а процесс облегченного раскрытия трещины в разных металлах и сплавах может быть вызван многими причинами: искажением под действием водорода кристаллической решетки металла, препятствующим диссипативному рассеянию энергии скопления дислокации за счет пластической деформации; образованием субмикроскопических выделений гидридов вследствие резкого увеличения концентрации водорода в области скопления дислокаций; снижением поверхностной энергии металла в результате выноса дислокациями водорода к микронесплошностям; повышением давления молекулярного водорода в несплошностях, приводящим совместно с концентраторами напряжений к преодолению сил сцепления в металле; снижением в участках повышенной концентрации водорода когезивной прочности металла. [29]
В СССР построены различные по принципу действия и инженерным масштабам установки для исследования поведения нагретого и ионизированного водорода в условиях, сходных с теми, которые, по нашим представлениям, будут иметь место в термоядерных реакторах. На этих установках сейчас ведутся исследования. [30]
Страницы: 1 2 3 4
