Поведение - различный газ
Cтраница 1
 |
Газовыделение маловязкого масла при различных условиях ионизации. [1] |
Поведение различных газов при ионизации весьма различно. Опыты в описанном выше приборе показали, что под действием приложенного напряжения к прибору, заполненному воз - духом, имеет место пони - жение давления ( рис. 32), ; очевидно, ( связанное с образованием озона. [2]
Поведение различных газов в общем одинаково. Различие ионизационных потенциалов ( см. § 193) приводит лишь к тому, что некоторые критические точки, о которых мы будем говорить ниже, осуществляются при других напряжениях и давлениях. [3]
Особенность поведения различных газов при горении весьма существенно влияет на развитие процесса горения в целом и определяет технику сжигания ( конструкции горелок и пр. [4]
Чтобы сравнивать поведение различных газов, удобно брать каждый из них в количестве одного моля. Если N - число Аво гадро, то Nm М - молекулярному весу газа. [5]
При исследовании поведения различных газов, близких по своим свойствам ( в определенных условиях) к идеальному, были, установлены основные закономерности, связывающие между собой параметры состояния и получившие название газовых законов. [6]
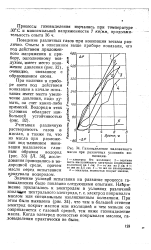
Как известно, в поведении различных газов наблюдаются большие отклонения от законов идеальных газов. Эти отклонения тем больше, чем ниже температура и выше давление, при которых находится газ. На рис. 4 показаны отклонения различных газов от закона Бойля - Мариотта при высоких давлениях. [7]
 |
Отклонения от законов идеальных газов. [8] |
Как известно, в поведении различных газов наблюдаются большие отклонения от законов идеальных газов. Эти отклонения тем больше, чем ниже температура и выше давление, при которых находится газ. На рис. 6 заметны отклонения различных газов от закона Бойля - Мариотта при высоких давлениях. [9]
Ввиду недостатка необходимых опытных данных для расчета свойств реальных газов была сделана попытка использования известного подобия в поведении различных газов в областях, близких к критическим. Это подобие натолкнуло на мысль выразить переменные свойства систем р, V и Т как доли я р / рн, Vnp V / Vi p и т Т / Ткр соответствующих критических констант для каждого газа, назвав их приведенными параметрами. Была высказана мысль, что подобие в поведении кривых, представляющих р - V - 7 -дашше, является показателем существования обобщенного, так называемого приведенного уравнения состояния, годного для всех газов, в которое все переменные, определяющие состояние газовой системы, входят в приведенной форме. [10]
Ввиду недостатка необходимых опытных - данных для расчета свойств реальных газов была сделана попытка использования известного подобия в поведении различных газов в областях, близких к критическим. Это подобие натолкнуло на мысль выразить переменные свойства систем р, V и Т как доли я р / р р, VHP V / VKV и т T / TKV соответствующих критических констант для каждого газа, назвав их приведенными параметрами. Была высказана мысль, что подобие в поведении кривых, представляющих р - V - Т - данные, является показателем существования обобщенного, так называемого приведенного уравнения состояния, годного для всех газов, в которое все переменные, определяющие состояние газовой системы, входят в приведенной форме. [11]
Различие между случаями, когда имеют место ограничения в свободе поступательного и вращательного движений, может быть установлено путем сопоставления поведения различных газов, включая благородные газы, молекулы которых не обладают вращательным движением. При обобщении полученных результатов мы обнаружили, что существенную роль играет также величина площадки, занимаемой одной молекулой. [12]
Ввиду недостатка необходимых данных для расчета свойств реальных газов была сделана попытка обобщения свойств реальных газовых систем путем использования известного подобия в поведении различных газов в областях, близких к критическим. [13]
N / V ( давления) газа способствует выполнимости классической статистики. Сравнивая поведение различных газов при одинаковых термодинамических условиях ( Т, р), мы должны учесть индивидуальные характеристики частиц. [14]
Как и во всех других случаях использования физических моделей, применимость модели идеального газа к тому или иному реальному газу зависит не только от свойств самого газа, но и от характера вопроса, на который требуется найти ответ. Такая модель не позволяет описать особенности поведения различных газов, но выявляет свойства, общие для всех газов. [15]
Страницы: 1 2