Аномальное поведение - вода
Cтраница 1
Аномальное поведение воды при указанных температурах объясняется следующим. [1]
 |
Электролитическая диссоциация воды. [2] |
Несмотря на аномальное поведение воды по отношению к показателю KW, можно сделать вывод, что содержащиеся в ней реагенты и сама вода повышают свою активность в отношении коррозии с повышением температуры до пределов, характерных для работы котлов высоких и сверхвысоких параметров. Этот вывод, очевидно, можно применить ко многим процессам коррозии. [3]
 |
Молекулярная ассоциация в жидкой фазе. [4] |
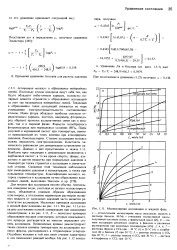
Для жидких фаз ассоциация вполне обычна. Аномальное поведение воды, учитывая ее низкую молекулярную массу, объясняется главным образом образованием олигомеров, а отклонение параметров растворов полярных веществ от идеальных значений часто является результатом ассоциации. Несколько примеров ассоциации в жидкой фазе показаны на рис. 1.11. На рис. 1.11 а показано достижение полной димеризации при повышении концентрации, а на рис. 1.11, б - несколько примеров образования высших олигомеров, которые показывают, что природа растворителя во многом определяет степень ассоциации. Приведенные кривые демонстрируют также сильное влияние температуры на ассоциацию молекул фенола, растворенного в тетрахлориде углерода. Подобные явления в той или иной степени характерны и для химических реакций вообще. [5]
Для жидких фаз ассоциация вполне обычна. Аномальное поведение воды, учитывая ее низкую молекулярную массу, объясняется главным образом образованием олигомеров, а отклонение параметров растворов полярных веществ от идеальных значений часто является результатом ассоциации. Несколько примеров ассоциации в жидкой фазе показаны на рис. 1.11. На рис. 1.11 а показано достижение полной димеризации при повышении концентрации, а на рис. 1.11, 6 - несколько примеров образования высших олигомеров, которые показывают, что природа растворителя во многом определяет степень ассоциации. Приведенные кривые демонстрируют также сильное влияние температуры на ассоциацию молекул фенола, растворенного в тетрахлориде углерода. Подобные явления в той или иной степени характерны и для химических реакций вообще. [7]
Гаузер, Бриджмэн и др. наблюдали интересную аномалию вязкости воды, заключающуюся в том, что ниже 30 при повышении давления вязкость вначале падает, а затем выше 1000 кГ / см2 начинает расти. Бриджмэн связывает аномальное поведение воды с влиянием давления на ассоциацию молекул. Выше 30, когда ассоциация молекул исчезает, эффекта не наблюдается. Однако причина этого явления не вполне выяснена. [8]
По данным табл. 17.3, очевидно, что число молекул незамерзающей воды ( Wnf) в большинстве случаев превышает число молекул Wfn, а количество Wfm, ассоциированной с дисахарид-ным звеном, мало или очень мало. Предполагается, что аномальное поведение воды в растворах является следствием взаимодействия ее молекул с ионизирующимися и полярными группами субстрата. Например, ионными группами гепарина являются карбоксильная, О - и N-сульфатные, а полярными - гидроксильные и полу-ацетальные. [9]
Поскольку Н - связи имеются не только в кристаллогидратах, но и в свободной воде, естественно, что в этом случае также было зафиксировано повышение рефракции примерно на 10 % от стандартного значения. Здесь уместно привести один пример, когда с помощью рефрактометрии удалось просто объяснить аномальное поведение воды при сверхвысоких давлениях. Так, ПП воды при сжатии давлением до 22 ГПа увеличивается от 1 33 до 1 60 вместе с увеличением ее электропроводности. Эти факты были объяснены некоторыми физиками предположением о приобретении водой металлических свойств при сверхвысоких давлениях. [10]
В частности, следовало бы отметить, что точка плавления льда понижается с увеличением давления. В этом отношении поведение воды отличается от поведения других веществ, так как в большинстве случаев точка плавления повышается с увеличением давления. Это аномальное поведение воды происходит вследствие того, что лед имеет меньшую плотность, чем вода, тогда как в большинстве случаев твердое тело плотнее жидкости. [11]
Рассмотрим цикл Карно с водой в качестве рабочего вещества. Температуры теплоотдатчика и тепло-приемника равны соответственно 6 и 2 С: при 6 С вода изотермически расширяется, а при 2 С - изотермически сжимается. Вследствие аномального поведения воды при 4 С при обеих температурах будет подводиться теплота и полностью превращаться в работу, что находится в противоречии со вторым началом. [12]
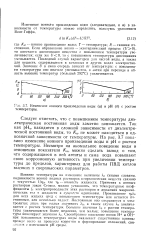 |
Изменение ионного произведения воды ( а и рН ( б с ростом температуры. [13] |
Следует отметить, что с повышением температуры диэлектрическая постоянная воды заметно понижается. Так как рНю находится в сложной зависимости от диэлектрической постоянной воды, то Kw не может находиться в однозначной зависимости от температуры. На рис. 3.7 показано изменение ионного произведения воды и рН с ростом температуры. Несмотря на аномальное поведение воды в отношении показателя Kw, можно сделать вывод о том, что содержащиеся в ней агенты и сама вода повышают свою коррозионную активность при увеличении температуры до пределов, характерных для работы ПВД котлов высоких и сверхвысоких параметров. [14]
Расстояние между ближайшими соседями равно 2 8 А; расстояние до соседей, следующих за ближайшими ( радиус второй координационной сферы), равно 4 5 А для льда с трид-вмитотюдобной структурой, тогда как в вварцепо-добной структуре этот радиус равен только 4 2 А. Вследствие этого и происходит увеличение плотности при плавлении. Из сравнения экспериментальных данных по угловому распределению интенсивности отраженных рентгеновских лучей с теоретически вычисленными зависимостями следует, что структуру воды нельзя считать строго кварцеподобной. Температурная зависимость углового распределения интенсивности рассеянного рентгеновского излучения показывает, что в первом приближении вода содержит три типа структур, однако эти структуры нельзя отделить друг от друга. При повышении температуры появляются области большей плотности с кварцеподобной структурой ( вода II), что приводит к повышению плотности вплоть до температуры 4 С. Между 0 и 4 С повышение плотности при превращении структур тридимитолоиобная - варцеподобная оказывается сильнее, чем общее разрыхляющее действие повышения температуры на структуру. Это приводит к аномальному поведению воды в указанном интервале температур. При комнатной температуре области с жварцеподобной структурой занимают уже большую часть объема воды. При более высоких температурах структура становится все более изотропной и молекулы Н2О стремятся к: более тесной упаковке. Однако не следует считать, что эти три типа пространственного расположения молекул воды соответствуют различным областям в ее объеме. Вода при всех температурах - гомогенная жидкость, и структуры воды типов I, II и III появляются только как результат среднестатистического взаимного расположения молекул. [15]
Страницы: 1