Поверхность - окислительный катализатор
Cтраница 1
Поверхность окислительных катализаторов в стационарном состоянии более однородна, чем поверхность свежеприготовленного катализатора. При введении добавок в катализатор изменяются не только его электронные свойства, но и неоднородность поверхности. Можно ожидать, что из большого набора участков, имеющихся на поверхности, всю работл будет выполнять одна какая-нибудь группа со значениями энер гии адсорбции, лежащими в узких пределах. Контролирующая стадия для этой группы участков будет контролирующей стадиел всего процесса. [1]
 |
Форма кристаллов молиб-дата висмута ( В12О3 - МоО3. [2] |
Таким образом, геометрия поверхности окислительных катализаторов влияет на окислительные превращения углеводородов. [3]
Изучение адсорбции кислорода и углеводородов на поверхности окислительных катализаторов полупроводников показало, что поверхность их неоднородна и теплоты адсорбции, энергии активации изменяются с заполнением. Следовательно, адсорбированные ион-радикалы закреплены на различных участках поверхности с различной прочностью связи. Перекисные радикалы связаны с поверхностью катализатора в одних случаях через атом углерода, а в других - через атом кислорода. Анализ адсорбционных данных показывает, что прочность этих связей для различных катализаторов не одинакова. [4]
Данные по гемолитическому изотопному кислородному обмену указывают на частичную диссоциацию кислорода на поверхности окислительных катализаторов. [5]
Построение более полных стадийных схем считаем преждевременным до получения надежных экспериментальных данных о лабильных формах, существующих на поверхности гетерогенных окислительных катализаторов. [6]
Две из четырех кислородных форм, обсуждаемых в этой главе, а именно О2 и СГ, имеют неспаренный электрон. Их при - сутствие на поверхности окислительных катализаторов должно обнаруживаться магнитными методами. Из данных по дифракции электронов, полученных Волом и Шишаковым для системы серебро - кислород, следует ожидать, что парамагнитные ионы О2 образуются в большом количестве. Это ожидание, однако, не было полностью подтверждено экспериментами. Так как метод ЭПР к таким металлам, как серебро, по-видимому, неприменим, парамагнетизм может быть обнаружен только косвенными методами. [7]
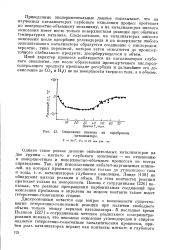 |
Окисление этилена на серебряном катализаторе. [8] |
Приведенные экспериментальные данные показывают, что на изученных катализаторах глубокого окисления процесс протекает по поверхностно-объемному механизму, а на катализаторах мягкого окисления имеет место только поверхностная реакция при обычных температурах катализа. Следовательно, на катализаторах мягкого окисления после адсорбции углеводорода и на поверхности любого окислительного катализатора образуется соединение с кислородом, вероятно, типа перекисей, которое затем окисляется до промежуточного стабильного продукта, десорбирующегося в объем. [9]
Измерение электронных характеристик катализаторов при хемосорбции смесей показало, что промежуточные формы заряжены положительно на катализаторах неполного окисления углеводородов и отрицательно на катализаторах глубокого окисления. Таков основной характер механизма окисления углеводородов, на основе которого следует рассмотреть, какими свойствами должна обладать поверхность окислительных катализаторов. [10]
НАК на этом образце должна возрастать, но кинетические данные показывают противоположный результат. Кроме того, реакцию окислительного аммонолиза можно проводить на фосфатах и сульфатах, в которых не существует таких дублетных центров из двух разнородных катионов. Поэтому нам представляется не обязательной дублетная модель поверхности окислительных катализаторов мягкого окисления углеводородов. [11]
Такая цепь превращения названа С. Рогинским [16] деструктивно-окислительным цепным механизмом, который является причиной образования продуктов глубокого окисления углеводородов. Скорость этой реакции больше скоростей образования кислородсодержащих продуктов ( альдегиды и другие) и поэтому избирательность процессов окисления углеводородов в большинстве случаев невелика. Для повышения избирательности необходимо изменить химический состав поверхности окислительных катализаторов путем введения добавок, что должно затормозить процесс деструктивного окисления. [12]
Страницы: 1