Поверхность - технический металл
Cтраница 1
Поверхность технических металлов, будучи неоднородной физически и химически, приводит к образованию на отдельных участках разных электродных потенциалов. Участки, где растворяются металлы, будут анодными, а участки, где разряжаются положительно заряженные ионы, - катодными. Таким образом, возникают гальванические микроэлементы, дающие электрический ток и вызывающие разрушение металла в случае, если он станет анодом. [1]
Поверхность технического металла состоит из большого числа микрогальванических элементов, которые вызывают усиленную коррозию основного металла. Теория локальных токов, предложенная Де ля Ривом, была первой теорией, объясняющей электрохимическую коррозию технических металлов. [3]
Вся поверхность технического металла представляет собой совокупность анодных и катодных участков. [5]
 |
Схема диффузии кислорода к одному катодному включению.| Схема дгффузии кислорода к нескольким катодным включениям. [6] |
Исследование поверхности технических металлов под микроскопом позволяет обнаружить зерна твердого раствора или химического соединения, по границам которых располагаются посторонние включения. Структурные составляющие имеют различные электродные потенциалы, поскольку они различны по химическому составу и по физическому состоянию. При погружении такого металла в раствор на границе электролита и каждой структурной составляющей образуется двойной слой и возникает скачок потенциала. [7]
В реальных условиях поверхность технического металла или сплава является обычно электрохимически неоднородной - отдельные участки ее ( анодные и катодные) обладают различными значениями электродного потенциала. Причины электрохимической неоднородности весьма многочисленны из-за включений, неоднородных и несплошных пленок из продуктов коррозии, напряжений различного рода и знака, различной концентрации компонентов-окислителей на отдельных участках. Таким образом, на поверхности технического металла или сплава возникают бесчисленные микрогальванические коррозионные элементы ( микропары), генерирующие коррозионный ток, суммарная величина которого определяет материальный эффект коррозии. [8]
Обозначим скорость выделения водорода на идеально чистом цинке через гп н - С такой скоростью водород будет выделяться на 99 % поверхности технического металла, приходящейся на долю цинка. [9]
В отличие от чистых металлов, поверхность которых с известными оговорками можно считать однородной, в особенности в случае жидкого металла, поверхность технических металлов существенно неоднородна как по химическому составу, так и по физико-химическим свойствам. В этом случае создаются условия для пространственного разделения катодного и анодного процессов - один из них легче протекает на одном участке металла, другой - на другом. [10]
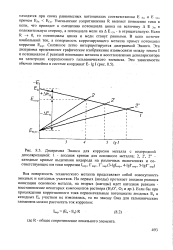
 |
Локальные токи в гальваническом элементе Zn-Cu для случая коррозии цинка с примесями меди. [11] |
Поверхность сплава также может быть химически неоднородной. Поэтому на поверхности технического металла в агрессивной среде имеются энергетически неоднородные участки с различными значениями потенциала. Таким образом, основной металл и примеси образуют множество коротко замкнутых микроскопических гальванических элементов. Наиболее опасны электроположительные примеси по отношению к основному металлу. [12]
Коррозионные процессы для идеально чистых металлов с однородной поверхностью могут одновременно протекать на любом ее участке. Вследствие неоднородности поверхности технических металлов различные ее участки неэквипотенциальны, что приводит к образованию электрохимических систем - ко-роткозамкнутых локальных ( местных) гальванических элементов. Процессы, вызывающие коррозию, происходят раздельно на анодных и катодных участках поверхности. [13]
Коррозионные процессы для идеально чистых металлов с однородной поверхностью могут одновременно протекать на любом ее участке. Вследствие не однородности поверхности технических металлов различные ее участки неэквипотенциальны, что приводит к образованию электрохимических систем - ко-роткозамкнутых локальных ( местных) гальванических элементов. Процессы, вызывающие коррозию, происходят раздельно на анодных и катодных участках поверхности. [14]
В реальных условиях поверхность технического металла или сплава является обычно электрохимически неоднородной - отдельные участки ее ( анодные и катодные) обладают различными значениями электродного потенциала. Причины электрохимической неоднородности весьма многочисленны из-за включений, неоднородных и несплошных пленок из продуктов коррозии, напряжений различного рода и знака, различной концентрации компонентов-окислителей на отдельных участках. Таким образом, на поверхности технического металла или сплава возникают бесчисленные микрогальванические коррозионные элементы ( микропары), генерирующие коррозионный ток, суммарная величина которого определяет материальный эффект коррозии. [15]
Страницы: 1 2