Поверхность - никель
Cтраница 1
Поверхность никеля должна быть вначале химически очищена путем погружения никелевой детали в раствор, содержащий 750 мл серной кислоты, 1 000 мл концентрированной азотной кислоты, 50 г хлористого натрия и 900 мл дистиллированной воды. После травления в этом растворе деталь следует тщательно промыть и высушить, после чего подвергать термообработке ( обезгаживанию) во влажном водороде при температуре 1 050 С в течение 30 мин. [1]
Поверхность никеля определена по паровой конверсии метана и кажущиеся константы скорости получены проточно-цирку-гранул. [2]
 |
Схема печи чернения. [3] |
Поверхность никеля является катализатором реакции разложения углеводородов на углерод и водород. Эта реакция протекает при 850 С. [4]
Поверхность никеля будем считать однородной и примем, что первая стадия является медленной, все остальные - быстрыми. Кроме того, предположим, что в области температур 800 - 900 С доля покрытия поверхности никеля радикалами СН2 незначительна. [5]
На поверхности никеля, палладия, платины молекулярный азот N2 образует комплексы с линейной конфигурацией: М - NN. [6]
На поверхности никеля марганцовистого, хромеля и нихрома восстановленная пленка состоит, в основном, из чистого никеля. [7]
На поверхности никеля, содержащего серу, значительно снижается перенапряжение водорода. Этим, вероятно, и объясняются низкие напряжения о растяжения в покрытиях, так как в соответствии с результатами работы [35] причиной возникновения таких напряжений является распад метастабильного твердого раствора водорода в металле. Сравнивая зависимости для о и ] / н, на рис. 41, видим, что увеличение содержания водорода в покрытии сопровождается повышением напряжений растяжения а. Увеличение о с повышением плотности тока может быть обусловлено и уменьшением количества серы в никеле, образующей равновесные сульфиды по границам зерен. При этом увеличивается объем системы и уменьшаются напряжения растяжения. [8]
На поверхности полублестящего никеля реакция протекает медленнее, изменение цвета менее заметно, а на поверхности тусклого никеля реакции вовсе не возникает. В основном, потемнение происходит в течение примерно 5 мин, но для блестящего никеля, содержащего чрезмерное количество блескообра-зующих добавок ( которые часто корродируют гораздо быстрее, чем обычно на практике), реакция может протекать значительно быстрее. [9]
Окисление поверхности никеля с соответствующим пассивации смещением потенциала в положительную сторону наблюдается и при насыщении щелочи газообразным кислородом. [10]
Водород на поверхности никеля, платины и подобных металлов активируется, диссоциируя на атомы, связанные с металлом... При этом, в согласии с мультиплетной теорией, нужно считать, что активный центр К состоит из двух атомов металла. [11]
При обновлении поверхности никеля величина перенапряжения водорода в растворе IN H2SO4, а также в IN H2SO4 с добавками 0ОШ КВг и при совместном добавлении 0ОШ КВг и 0ОШ сульфата тетрабутиламмония одинакова. Можно полагать, что при достаточно интенсивном обновлении поверхности ионы Вг - и тетрабутиламмония, адсорбирующиеся на поверхности никелевого электрода, а также разрядившийся водород тотчас удаляются с поверхности металла механическим путем и поэтому не влияют на перенапряжение выделения водорода. [13]
Окись углерода на поверхности никеля адсорбируется в виде молекул. Установлено существование пяти форы связи со с поверхностью никеля, различных по структуре и силе связи, зависящих от кристаллической структуры никеля и условий процесса. Исследования контактной разности потенциалов показали, что окись углерода в интервале температур 75 - 250 С снижает работу выхода на глтализаторе, т.е. слой хемсорбированного газа в условиях протекания процесса гидрирования со заряжен положительно. [14]
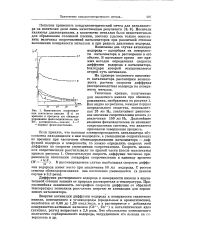 |
Зависимость сопротивлэ - ная 25 мл Ш, увеличивает равновес-ния скелетного никеля ( 3 г от значение сопротивления вплоть до. [15] |
Страницы: 1 2 3 4 5
