Однородная поверхность - адсорбент
Cтраница 1
Однородная поверхность адсорбента может не быть равной в энергетическом отношении. Поверхность адсорбента имеет закономерно расположенные точки, в которых адсорбированные молекулы удерживаются более прочно, чем в промежутках ( провалах) между ними. Поверхность можно считать однородной, если теплота адсорбции одинакова в каждой точке. [1]
Представим себе однородную поверхность адсорбента, находящуюся при постоянной температуре в контакте с газом. Равновесие устанавливается тогда, когда число молекул адсорбата, остающихся на поверхности в единицу времени, становится равно числу молекул, покидающих поверхность за то же время. Число молекул, остающихся на адсорбенте, пропорционально концентрации С и доле поверхности, которая остается свободной. Если вся рассматриваемая поверхность имеет площадь, равную единице, и занята ее доля, равная 0, то доля ( 1 - 0) свободная. [2]
Это соответствует энергетически однородной поверхности адсорбента. [3]
Межмолекулярные взаимодействия адсорбат - адсорбат на однородной поверхности адсорбента. [4]
Ленгмюра уравнение адсорбции - описывает равновесие на однородной поверхности адсорбента при отсутствии межмолекулярных взаимодействий ад-сорбата. [5]
Ленгмюра уравнение адсорбции - описывает равновесие на однородной поверхности адсорбента при отсутствии межмолекулярных взаимодействий адсорбата. [6]
Лснгмюра уравнение адсорбции - описывает равновесие на однородной поверхности адсорбента при отсутствии межмолекулярных взаимодействий адсорбата. [7]
Ленгмюра уравнение адсорбции ( 160 - 163) описывает равновесие на однородной поверхности адсорбента при отсутствии межмолекулярных взаимодействий адсорбата. [8]
Согласно электронной теории хемссорбции, молекулы одного и того же газа могут связываться с энергетически однородной поверхностью полупроводникового адсорбента различными типами связи, между которыми существуют переходы. На основе статистического метода Гиббса для систем с переменным числом частиц получены выражения для концентраций хемосорбированных частиц с каждым данным типом связи. Эти выражения содержат химический потенциал адсорбируемых частиц в газовой фазе, уровень Ферми для электронов адсорбента, энергии, соответствующие каждому типу связи и кратности вырождения состояний адсорбированных частиц. [9]
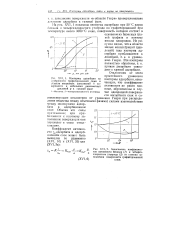
Отклонения от этого простейшего уравнения изотермы адсорбции, означающие, что коэффициент активности не равен единице, обусловлены в случае однородной поверхности адсорбента ( как и соответствующие отклонения от уравнения Генри при распределении вещества между объемными фазами) силами взаимодействия между молекулами адсорбата в адсорбционном слое. Обычно это силы притяжения; при приближении к плотному заполнению поверхности они переходят в силы отталкивания. [11]
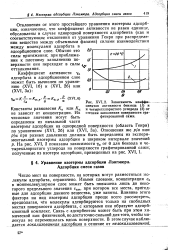 |
Зависимость коэффициентов активности бензола ( 1 и и четыреххлористого углерода ( 2 от. [12] |
Отклонения от этого простейшего уравнения изотермы адсорбции, означающие, что коэффициент активности не равен единице, обусловлены в случае однородной поверхности адсорбента ( как и соответствующие отклонения от уравнения Генри при распределении вещества между объемными фазами) силами взаимодействия между молекулами адсорбата в адсорбционном слое. Обычно это силы притяжения; при приближении к плотному заполнению поверхности они переходят в силы отталкивания. [13]
При достаточно больших концентрации или давлении газа наступают отклонения от закона Генри из-за неравенства коэффициента активности уа единице. Неравенство в случае однородной поверхности адсорбента обусловлено силами взаимодействия между молекулами адсорбата в адсорбционном слое. Наиболее часто это силы притяжения; при приближении к предельному заполнению адсорбционного слоя они переходят в силы отталкивания. [14]
При достаточно больших концентрации или давлении газа наступают отклонения от закона Генри из-за неравенства коэффициента активности - уа единице. Неравенство в случае однородной поверхности адсорбента обусловлено силами взаимодействия между молекулами адсорбата в адсорбционном слое. Наиболее часто это силы притяжения; при приближении к предельному заполнению адсорбционного слоя они переходят в силы отталкивания. [15]
Страницы: 1 2