Повышение - анодная плотность - ток
Cтраница 3
При электрохимическом оксидировании скорость растворения металла и образования окисла определяется не только составом раствора, но и электрическим режимом процесса. Повышение анодной плотности тока ускоряет растворение железа и образование центров кристаллизации. Более толстые оксидные пленки получаются при сравнительно низких плотностях тока. [31]
При анодном оксидировании скорость формирования оксидной пленки зависит не только от состава и температуры электролита, но и от режима электролиза. Повышение анодной плотности тока ускоряет реакцию ионизации железа и образования центров кристаллизации оксида. [32]
При повышении температуры скорость травления увеличивается, особенно в слабокислых растворах. С повышением анодной плотности тока скорость травления увеличивается и уменьшаются потери металла за счет уменьшения растворения железа. После анодного травления в растворах солей и слабокислых растворах на поверхности изделий остается шлам, который должен быть удален при последующей обработке. Хорошие результаты можно получить, применяя ранее указанный способ травления в азотной, хромовой и соляной кислотах. [33]
Плотность тока зависит от материала анода. При повышении анодных плотностей тока выход гипохлорита натрия по току несколько снижается и возрастает выход хлората по току. [34]
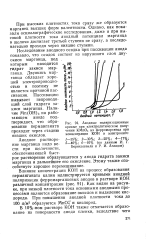 |
Анодные поляризационные кривые при электролитическом получении КМпО4 из ферромарганца при концентрации КОН в электролите. [35] |
Как видно на рисунке, при низкой плотности тока основными анодными процессами являются образование окислов и выделение кислорода. При повышении анодной плотности тока до 100 а / м2 образуются МпОГ и кислород. [36]
Режим анодного травления также играет важную роль в создании пористости. Так, повышение анодной плотности тока приводит к увеличению ширины и глубины каналов Повышение температуры способствует уменьшению ширины каналов и увеличению их густоты. [37]
Наряду с растворением титана переходят в расплав марганец и алюминий. С; повышением анодной плотности тока переход марганца в расплав уменьшается, поскольку потенциал марганца более электроотрицателен, чем потенциал всех других металлов, присутствующих в анодном материале - Ti, Al, Fe и др. Переход алюминия в расплав начинается при Da - 0 l а / см2, с повышением анодной плотности тока его количество в расплаве увеличивается. В пределах Da 0 4 - 0 6 а / см2 наблюдается максимальное количество алюминия в расплаве. [38]
Величина анодной плотности тока оказывает существенное влияние на интенсивность процесса анодного окисления марганца. Установлено, что повышение анодной плотности тока по отношению к катодной способствует понижению скорости этого нежелательного процесса. Поэтому анодную плотность тока поддерживают примерно в 2 раза более высокой, чем катодную. Достигается это перфорированием анодов. [39]
Понижение концентрации серной кислоты связано с возрастанием доли тока, расходуемой на побочную электрохимическую реакцию выделения кислорода на аноде. Характерно, что при повышении анодной плотности тока концентрация серной кислоты, при которой начинается образование пероксодвусерной кислоты, уменьшается. [40]
По имеющимся данным, электролиты на основе станната калия более стабильны, чем электролиты на основе станната натрия, так как менее подвержены гидролизу. Следует отметить, что с повышением анодной плотности тока растворимость оловянных анодов в калиевых электролитах заметно снижается. В связи с этим было предложено использовать оловянные аноды, содержащие около 1 % алюминия. Аноды из сплава олова с алюминием, так же как оловянные аноды, в процессе работы должны быть покрыты пассивной пленкой. [41]
 |
Электролизер для по. [42] |
Анодное растворение ферромарганца осуществляют в 17 - 25 % - ном растворе КОН. Выход перманганата калия по току увеличивается с повышением анодной плотности тока. Катодная плотность тока не оказывает существенного влияния на процесс. Повышение температуры приводит к снижению выхода по току в основном за счет разложения перманганата калия. [43]
Существенное влияние на выход по току хлора ( ВтС1) оказывает концентрация хлоридов. Зависимость Вт01 от концентрации Nad показана на рис. 4.21. Повышение анодной плотности тока при низких концентрациях NaCl резко увеличивает ВтС1, поэтому с увеличением плотности тока следует ожидать увеличения скорости окисления органических загрязнений. Однако необходимо заметить, что, поскольку между величиной тока и напряжением в растворе существует известная зависимость, выражаемая законом Ома ( U3 IR), увеличение / неизбежно приведет к увеличению иэ, и, следовательно, возрастут затраты электроэнергии на обработку воды. Таким образом, выбор оптимальных величин плотностей тока и напряжения между электродами при электрохимической очистке воды весьма существен. [44]
Сила тока элемента не соответствует непосредственно увеличению скорости коррозии. Она только вызывает сдвиг потенциала в положительную сторону и вследствие этого повышение парциальной анодной плотности тока. [45]
Страницы: 1 2 3 4