Повышение - растворимость
Cтраница 1
Повышение растворимости в ряде случаев наблюдается при температурах значительно ниже тех, при которых термодинамически возможно разрушение валентных связей иеяСЛУ фрагментами угля. [1]
Повышение растворимости PbS04 в присутствии названных веществ объясняется образованием с ними более слабо диссоциирующих соединений ( например, образованием мало диссоциированного ацетата свинца при добавлении ацетат-ионов) и отчасти образованием комплексов. [2]
Повышение растворимости в воде малорастворимого электролита при добавлении солей, не содержащих общих с ними исков, может быть объяснено понижением коэффициента активности в разбавленных растворах по мере роста ионной силы. [3]
Повышение растворимости часто можно объяснить взаимодействием между компонентами. Если образуется малопрочный комплекс, то растворимость возрастает незначительно. [4]
Повышение растворимости с увеличением температуры объясняют тем, что в металле растворяются не молекулы Н2, а атомы, количество которых в равновесной системе Н2 5 2Н с увеличением температуры растет. [5]
Повышение растворимости PbS04 вТприсутствии названных веществ объясняется образованием с ними более слабо диссоциирующих соединений ( например, образованием мало диссоциированного ацетата свинца при добавлении ацетат-ионов) и отчасти образованием комплексов. [6]
Повышение растворимости азота в твердом металле и связыва ние его в стойкие нитриды обеспечивают дополнительным легиро ванием металла шва титаном, алюминием, церием и цирконием. [7]
Повышение растворимости осадков в присутствии электролитов называется солевым эффектом. [8]
Повышение растворимости PbS ( 4 в присутствии названных веществ объясняется, образованием с ними более слабо диссоциирующих соединений ( например, образованием мало диссоциированного ацетата свинца при добавлении - ацетат-ионов) и отчасти образованием комплексов. [9]
 |
Диаграмма состояния системы TiCU - NbCU - AlCb. [10] |
Повышение растворимости хлоридов в четыреххлористом титане в присутствии другого хлорида, дающего с первым более или менее легкоплавкую эвтектику, очень велико. [11]
Повышение растворимости белков в растворе нейтральных электролитов слабых концентраций может быть объяснено образованием соединений между ионом электролита и белка. [12]
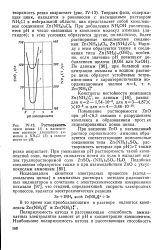 |
Растворимость окиси цинка ( / в насыщенном растворе хлористого аммония и NH4C1 ( 2 в зависимости от рН. [13] |
Повышение растворимости ZnO при рН6 3 связано с разрушением комплекса и образованием прост лх гидратированных ионов цинка. [14]
Повышение растворимости ацетилена позволяет снизить расход абсорбента, а применение более летучих растворителей - температурный уровень перегонки, вследствие чего уменьшается расход тепла на регенерацию абсорбента. Наряду с этим появляются дополнительные расходы на охлаждение до низких температур, но эти расходы значительно меньше, чем экономия энергии на регенерацию абсорбента. [15]
Страницы: 1 2 3 4