Повышение - степень - окисление
Cтраница 3
Несмотря на то, что при повышении степени окисления путем добавления NO2 начальная концентрация окислов азота в газе возрастает, в отходящих газах после очистки остаточное содержание окислов азота будет таким же, как и при окислении NO до NO2 в окислительных объемах. Таким образом, метод дозирования NO2 может быть применен вместо окисления NO в окислительных объемах. [31]
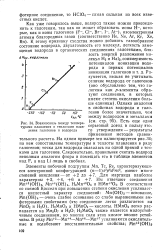 |
Взаимосвязь между температурами плавления и теплотами плавления галогенов и водорода. [32] |
В соответствии со схемой Косселя при повышении степени окисления усиливается кислотный характер соединений: Мп ( ОН) 2 - основание, Мп ( ОН) 4 - очень слабое основание со слабо выраженными ам-фотерными свойствами ( это соединение легко разлагается на МпО2 и Н2О), Н2МпО4 и НМпО4 - кислоты. [33]
В соответствии со схемой Косселя при повышении степени окисления усиливается кислотный характер соединений: Мп ( ОН) 2 - основание, Мп ( ОН) 4 - очень слабое основание со слабо выраженными амфотерными свойствами ( это соединение легко разлагается на МпО2иН2О), Н2МпО4 и НМпО4 - кислоты. [34]
Окислением называется процесс отдачи электронов, сопровождающийся повышением степени окисления. [35]
Как изменяются кислотно-основные свойства соединений марганца при повышении степени окисления этого элемента. [36]
Последняя реакция уникальна, так как здесь происходит повышение степени окисления металла. [37]
Как изменяются кислотно-основные свойства оксидов и гидроксидов с повышением степени окисления таллия. [38]
Анализ изменения кислотно-основных свойств соединений марганца показывает, что с повышением степени окисления основные свойства элемента уменьшаются, а кислотные свойства возрастают. В высоких степенях окисления кислотные свойства ярко выражены, а атом элемента служит кислотообразователем. [39]
Марганец образует несколько оксидов, характер которых постепенно меняется: по мере повышения степени окисления они проявляют более кислотные свойства. Оксид МпО растворим в кислотах с образованием солей розоватого цвета. При подщелачивании растворов из них выпадает оксид Mn ( OH) s, быстро окисляющийся на воздухе до образования смеси МпО ( ОН), Mn2O3, Н2МпО3, и раствор приобретает коричневый цвет. Процесс окисления протекает практически нацело, и это служит в некоторых случаях для количественного определения концентрации растворенного з зоде кислорода. Оксиду Мп2О3 соответствует нерастворимый в воде гид-роксид Мп ( ОН) 3, являющийся слабым основанием. Его гидроксид Мп ( ОН) 4 растворяется как в кислотах, так и в щелочах, хотя и там, и там неохотно. [40]
Можно ожидать, что МпО4 - проявляет окислительно-восстановительные свойства соответственно понижению и повышению степени окисления Мп. [41]
Можно ожидать, что MnO - проявляет окислительно-восстановительные свойства соответственно понижению и повышению степени окисления Мп. [42]
Окислением называют отдачу веществом ( атомом, ионом или молекулой) электронов, сопровождающуюся повышением степени окисления. [43]
Влияние двухступенчатости процесса окисления аммиака в присутствии окисных кобальтового и железо-висмут-марганцевого катализаторов выражается в повышении степени окисления аммиака и в возможности работы при более высоких объемных скоростях. [44]
Таким образом, даже для благородного газа - ксенона - можно видеть, что при повышении степени окисления стабильность бинарных соединений уменьшается, их окислительная активность растет, а устойчивость ацидокомплексов в этом направлении повышается. [45]
Страницы: 1 2 3 4