Повышение - щелочность
Cтраница 1
Повышение щелочности и минерализации водных сред способствует еще большему снижению контактно-усталостной прочности долот-ной стали. [1]
Повышение щелочности увеличивает стехиометрический коэффициент п; при [ ОН - ] 0 2 моль / л ухудшается качество покрытий. Увеличение концентрации глюкозы выше определенного предела ( 1 3 г / л инвертированного сахара) уменьшает максимальную толщину покрытия. С ростом концентрации аммиака снижается начальная скорость серебрения, но вместе с тем увеличивается стабильность раствора и толщина покрытия. Поэтому не следует опасаться некоторого избытка аммиака сверх необходимого для связывания ионов серебра. [2]
Повышение щелочности увеличивает стехиометрический коэффициент п; при [ ОН - ] 0 2 моль / л ухудшается качество покрытий. Увеличение концентрации глюкозы выше определенного предела ( 1 3 г / л инвертированного сахара) уменьшает максимальную толщину покрытия. С ростом концентрации аммиака снижается начальная скорость серебрения, но вместе с тем увеличивается стабильность раствора и толщина покрытия. Поэтому не следует опасаться некоторого избытка аммиака сверх необходимого для связывания ионов серебра. Повышение температуры значительно ускоряет восстановление серебра - Еа 110 кДж / моль. Однако при этом ускоряется и реакция в объеме раствора. [3]
Повышение щелочности у катодных участков приводит к растворению оксидной пленки, и покрытие становится анодом. [4]
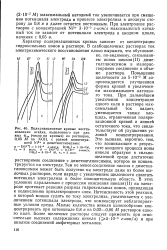 |
Поляризационные кривые восстановления осадка, выделенного при разных фэл ( числа на кривых из растворов, 0 05 М по КОН, с разной концентрацией Ni2 и диметилглиоксима. [5] |
Повышение щелочности до 5 - 10 - 2 М сопровождается улучшением формы кривой и увеличением максимального катодного тока. При дальнейшем увеличении концентрации едкого кали в растворе максимальный ток падает, уменьшается также площадь, ограниченная поляризационной кривой и линией остаточного тока, что свидетельствует об ухудшении условий концентрирования. Это вызвано, вероятно, тем, что возникающие в результате анодного процесса ионы никеля образуют в сильнощелочной среде достаточно растворимое соединение с диметилглиоксимом, которое не концентрируется на электроде. Тем не менее соединение никеля с диметилглиоксимом может быть получено на электроде даже из более щелочных растворов, если наряду с увеличением щелочности сдвигать потенциал электролиза в более положительную область. В этих условиях параллельно с процессом окисления никеля ( II) на электроде протекает реакция разряда гидроксильных ионов, приводящая к подкислению приэлектродного слоя. Интенсивность этой реакции, о которой можно судить по току электролиза, увеличивается с увеличением потенциала электрода, что компенсирует неблагоприятные условия среды. Малые количества никеля целесообразно концентрировать при потенциале 0 8 в из 0 02 - 0 06 М растворов едкого кали. Более щелочные растворы следует применять при относительно высоких содержаниях никеля ( 5 - 10 - 6 г-ион / л) и при анализе соединений амфотерных металлов. [6]
Повышение щелочности и понижение температуры массы при сочетании способствуют вступлению диазогруппы в пара-положение к окси-группе И-кислоты, в результате чего образуется побочный л-оксидисазокраситель более синего оттенка. [7]
Повышение щелочности и понижение температуры массы при сочетании способствуют вступлению диазогруппы в пара-положение к окси-группе И-кислоты, в результате чего образуется побочный n - оксидисазокраситель более синего оттенка. [8]
Повышение щелочности раствора снижает концентрацию водородных ионов и соответственно увеличивает концентрацию ионов пергидроксила. Поэтому с повышением рН раствора возрастает и скорость отбеливания. [9]
 |
Аппарат для зонной очистки. [10] |
Повышение щелочности раствора также снижает выход по току. Полученный электролизом металл промывают дистиллированной водой, а затем соляной кислотой при нагревании. Это позволяет отмыть примеси цинка, меди, свинца, железа и некоторых других металлов. Иногда применяют последовательную обработку соляной и азотной кислотами. После промывки металл обычно содержит 99 9 - 99 95 % галлия. [11]
Повышение щелочности раствора гипохлорита приводит к замедлению процесса отбелки и при прочих равных условиях к уменьшению белизны волокна. Поэтому необходимо не только контролировать концентрацию активного хлора в ванне, но и периодически определять рН среды. [12]
Повышение щелочности котловой воды и нарушение солефос-фатного соотношения приводят к росту содержания водорода в паре. [13]
Повышение щелочности раствора перекиси снижает концентрацию водородных ионов и увеличивает концентрацию пергидроксильных. Например, целлюлозные волокнистые вещества в сильнощелочной среде подвергаются, хотя и медленно, действию кислорода, что приводит к снижению длины цепи целлюлозных молекул и как следствие-к снижению прочности. Поэтому операции отбелки необходимо проводить таким образом, чтобы снизить до минимума разложение перекиси с выделением кислорода, например вызываемое мельчайшими примесями таких металлов, как железо, медь и марганец. Различные виды материалов, подвергаемых отбелке, целесообразно разбить на две группы: на состоящие в основном из целлюлозы и на имеющие преимущественно белковую структуру. [14]
Повышение щелочности питательной воды может привести к переходу от режимов чистофосфатной щелочности к щелочно-солевому режиму при неизменных условиях дозирования смешанного раствора фосфатов. Если при этом концентрации фосфатов и относительная щелочность остаются в пределах норм ПТЭ, то такое отклонение от режима чистофосфатной щелочности не рассматривается как нарушение водного режима, так как оба фосфатных режима считаются неопасными в отношении щелочной коррозии. К серьезным последствиям могут привести нарушения режима чистофосфатной щелочности в сторону занижения рН котловой воды, например в результате передозировки кислых фосфатов. При таких нарушениях создаются условия для интенсивной коррозии металла с водородной деполяризацией и возникает опасность образования железофосфатных накипей, особенно в солевых отсеках котлов со ступенчатым испарением, где концентрация фосфатов, естественно, выше. [15]
Страницы: 1 2 3 4 5