Поглощение - водород
Cтраница 3
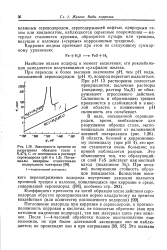 |
Зависимость времени до разрушения образцов стали с 0 47 % С от потенциала в растворе сероводорода ( рН 4 и 1 3. Потенциалы измерены относительно водородного электрода. [31] |
Поглощение водорода при коррозии в сероводороде, в противоположность коррозии в кислотах, не полностью обратимо ( как при катодном выделении водорода), так как материал здесь уже изменен. [32]
Поглощение водорода сталью не ограничивается растворимостью ( 3 - 10 - 8 моля. [33]
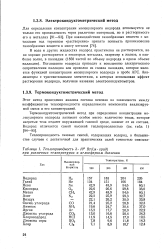 |
Теплопроводность Я 103 Вт / ( м град. [34] |
Поглощение водорода приводит к повышению электрического, сопротивления палладия или проволок из сплава палладия, которое является функцией концентрации молекулярного водорода в пробе АГС. Анализаторы с чувствительными элементами, в которых использован эффект растворения водорода, получили название электрокондуктометров. [35]
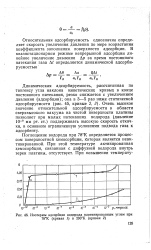 |
Изотермы адсорбции водорода платинированным углем при 78 К ( кривая / и 293 К ( кривая 2. [36] |
Поглощение водорода при 78 К определяется процессом поверхностной хемосорбции, Которая является неактивированной. При этой температуре активированная хемосорбция, связанная с диффузией водорода внутрь зерен платины, отсутствует. [37]
Поглощение водорода литием может идти и при более низких температурах, причем здесь важную роль играет чистота поверхности. Возогнанный литий при комнатной температуре поглощает за сутки 9 мол. [38]
Поглощение водорода начинается уже при 320 С. При 680 С оно идет очень энергично и реакция быстро доходит до конца. [39]
Поглощение водорода рением изучено мало. [40]
Поглощение водорода ( табл. 73) наблюдается [ три нагревании металлов в водороде при температурах выше 200 - 300 С, а также в том случае, когда водород электролитически выделяется на катодах из тантала или ниобия. [41]
Поглощение водорода литием начинается при температуре около 420 С и бурно протекает при 710 С [67, 68], взаимодействие водорода с натрием начинается при температуре, близкой к точке плавления. Калий начинает заметно взаимодействовать с водородом при 200 С, а рубидий и цезий - при 100 С; в препаративной технике их получают при 300 - 350 С. Чистый гидрид лития плавится при 680 С, NaH - под давлением при 800 С, RbH разлагается при 300 С, a CsH полностью разлагается при 389 С. Гидриды растворяются в соответствующих металлах. Натрий, например, при температуре 250 С растворяет около 0 003 % NaH, а при 400 С - около 1 5 % NaH. Растворение сопровождается диссоциацией гидрида на металл и атомарный водород, который в таком виде остается в металле. В таких случаях в защитной подушке инертного газа ( аргона) устанавливается равновесное парциальное давление водорода. Если жидкий металл - теплоноситель загрязнен гидридами, то на охлаждаемых поверхностях теплообменника возможно выделение твердых частичек гидридов, что приведет к уменьшению теплоотдачи, а также диффузия водорода в металл стенки и изменение его механических и теплофизических свойств. [42]
Поглощение водорода создает значительные искажения кристаллической решетки и резко ухудшает механические свойства металла. Последующий нагрев способствует удалению значительной части поглощенного водорода. Электрохимическое поведение железа и никеля, полученных электролизом водных растворов, отличается от поведения тех же металлов после переплавки, во время которой водород удаляется. [43]
Поглощение водорода титаном и торием, Новосибирск, 1960, Автореф. [44]
Поглощение водорода металлом продолжается до тех пор, пока в системе не установится равновесное давление, соответствующее упругости водорода над сплавом, получившейся в результате насыщения концентрации. Равновесное давление водорода повышается с увеличением концентрации водорода в металле. [45]
Страницы: 1 2 3 4