Поглощение - двуокись - азот
Cтраница 1
Поглощение двуокиси азота азотной кислотой происходит в поглотительных башнях при температуре минус 10 - минус 12 С. [1]
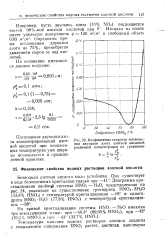 |
Коэфициенты скорости поглощения двуокиси азота азотной кислотой различной концентрации из уравнения. [2] |
Поглощение двуокиси азота концентрированной азотной кислотой при пониженных температурах уже широко используется в промышленной практике. [3]
Для поглощения двуокиси азота применяют порошок огнеупорного шамота с размером зерен 0 8 - 1 6 мм, обработанный 10 % - ным спиртовым раствором дифениламина из расчета 0 7 мл раствора на 1 г порошка. Приготовленный порошок высушивают при комнатной температуре, помещают в ампулы и запаивают их. [4]
Для поглощения двуокиси азота применяют порошок огнеупорного шамота с диаметром зерен 0 8 - 1 6 мм, обработанный 10 % - ным спиртовым раствором дифениламина из расчета 0 7 мл раствора на 1 г порошка. Приготовленный порошок высушивают при комнатной температуре, помещают в ампулы и запаивают их. [5]
После поглощения двуокиси азота раствором едкого натра можно оттитровать образовавшийся в растворе нитрит. [6]
Процесс поглощения двуокиси азота проводится в три ступени при температуре около - 10 С. В первой ступени колонны циркулирует кислота, содержащая до 30 % двуокиси азота, во второй - до 20, в третьей - до 10 % NO2 - В верхнюю часть колонны подается свежая, предварительно охлажденная до - 10 С азотная кислота. [7]
Реакция поглощения двуокиси азота водой является обратимой, и положение равновесия зависит от концентрации азотной кислоты, давления и температуры. Разбавленная азотная кислота полностью поглощает двуокись азота с одновременным выделением окиси азота, в то время как концентрированная кислота в присутствии даже небольшого количества окиси азота перестает поглощать двуокись азота. [8]
Процесс поглощения двуокиси азота водой при атмосферном давлении заканчивают, когда концентрация окислов азота в газах достигнет 1 %, после чего газы промывают раствором соды. [9]
Лроцесс поглощения двуокиси азота проводится при температуре около - 10 в три ступени. В верхнюю часть колонны подается свежая, предварительно охлажденная до - 10 азотная кислота. Каждая ступень поглощения имеет два слоя насадки: верхний слой орошается перетекающим раствором, нижний - раствором, циркулирующим при помощи насосов. Насыщенный двуокисью азота раствор азотной кислоты отводится из ижней ступени в отбелочную колонну 18, отходящие газы поступают в аппарат 17, где промываются разбавленной азотной кислотой ( из газового холодильника 8), предварительно отбеленной продувкой воздухом от растворенных окислов азота. Промыватель газов 17 работает без охлаждения. Вследствие поглощения паров кислоты и частично двуокиси азота кислота укрепляется до содержания HNO3 40 % и отводится в смеситель сырой смеси. Окончательная промывка газов производится водой в этом же аппарате 17 на верхнем слое насадки. Разбавленная кислота выводится из системы и после нейтрализации сливается в канализацию или используется в другом производстве. Из раствора окислов азота в азотной кислоте в отбелочной колонне 18, снабженной паровой рубашкой, отгоняется чистая двуокись азота. Азотная кислота после охлаждения в холодильнике 19 собирается в сборник 20, откуда часть ее выводится как продукционная кислота. Оставшаяся кислота возвращается в цикл на поглощение NO2 из газов. [10]
 |
Общий вид контактного отделения. [11] |
Процесс поглощения двуокиси азота проводится при температуре около - 10 в три ступени. [12]
 |
Растворимость МО2 в безводной HNO3. [13] |
При поглощении двуокиси азота азотной кислотой однородный раствор образуется только до насыщения кислоты при данной температуре. При введении большего количества двуокиси азота образуется новая жидкая фаза, и система получается уже двуслойной. [14]
Равновесная степень поглощения двуокиси азота растворами азотной кислоты при 35 С представлена на рис. Х-14. Из этой диаграммы следует, что при парциальном давлении двуокиси азота 0 1 ат получение азотной кислоты, имеющей концентрацию более 60 % HNO3, практически затруднительно. [15]
Страницы: 1 2 3 4