3-эпимер
Cтраница 1
Сравнение 3-эпимеров в ряду андростерона, андростандиола и андро-стендиола показывает, что За-оксистероиды неизменно превосходят по активности соответствующие Зр-соединения. Лумиандростерон ( VII), 13-эпимер андростерона, образующийся при облученииа18 последнего ультрафиолетовым светом, неактивен. При ацетилировании андростерона активность уменьшается лишь незначительно; ацетат, однако, обладает заметно более продолжительным действием. [1]
Эпимеры дают положительную реакцию в мягких условиях, в то время как 3-эпимеры окраски не дают. Так как реакция с минеральными кислотами, очевидно, заключается в дегидратации спиртов, то [ 3-соединения, испытывающие меньшие пространственные затруднения, повидимому дегидратируются не так легко, как их 17а - эпимеры. Ни один из эпимерных тестостеронов или 17-дигидроэквиленинов не образует нерастворимого дигитонида. [2]
Из-за наличия аксиального замещения в индольной системе колец соединения псевдоряда ( 211) всегда менее устойчивы, чем их 3-эпимеры нормального ряда, у которых С-2 расположен экваториально. [3]
Образующийся при этом в качестве побочного продукта 17а - эстрадиол примерно в 40 раз менее активен, чем природный 17 3-эпимер. [4]
В первом случае в смеси слегка преобладает квазиаксиальный 12а - эпимер, а во втором случае основным продуктом реакции является квазиэкваториальный 12 3-эпимер. [5]
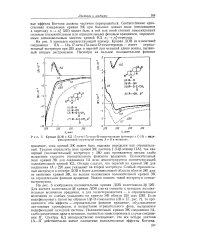 |
Кривые ДОВ и КД 17-кето - 17а - окса - В-гомостероидов ( эпимеры у С-13 с модифицированной структурой колец Л и В в метаноле. [6] |
Труднее определить знак кривой ЭК лактона I ( 13 3-эпимер ПА), так как первый ( положительный) экстремум у 260 ммк проявляется весьма слабо вследствие сильного отрицательного фонового вращения. Положительный знак кривой ЭК для соединения IA ясно демонстрируется соответствующей положительной кривой КД. Отсюда следует, что перегиб на кривой ЭК Для соединения IA у 220 ммк указывает на второй экстремум. Слабый отрицательный экстремум в спектре ДОВ в более длинноволновой области вблизи 280 ммк не свойствен кривой ЭК, но вызван наложением положительной кривой ЭК на отрицательное фоновое вращение. [7]
Путем гидрирования над родиевым катализатором, расщепления фе-нольного эфира и N-ацетилирования этот нитрон был превращен в фенол ( 266), имеющий надлежащую стереохимию пирролидинового кольца. Следующей задачей было превращение вес-соединения ( 268) в природный 8 3-эпимер. [8]
Бенедикта привели к 5 6-дикетону, метиловый эфир енольной формы которого ( 271; 8а -) был превращен в 8р - эпимер кипячением с 10 % - ной водной щелочью. Гидрирование, обработка кальцием в жидком аммиаке, ре-ацетилирование и окисление позволили получить 8 3-эпимер соединения ( 268), который был превращен в соответствующий еноллактон, легко образующий пентациклический кетон ( 270) при обработке магнийиодме-тилом. [9]
Данные по измерению скоростей окисления аллиловых спиртов следует интерпретировать с осторожностью, так как в некоторых случаях окисление псевдоаксиальных изомеров может протекать необычным образом, как это следует из результатов, сообщенных Эшенмозером. Так, в то время как окислеиие Д4 - холестанола - 6а хромовым ангидридом в уксусной кислоте приводит с хорошим выходом к соответствующему а р-ненасыщенному кетону с потреблением 1 моля окислителя, его 6 3-эпимер реагирует в тех же условиях быстрее, причем расходуется 2 моля окислителя. [10]
При изучении моделей Рейхштейн наблюдал, что метиленовая группа при С1г экранирует эфирную группу при С17 примерно в такой же степени, как и угловая метильная группа. Таким образом, между 17-оксисоединениями и 17-эфирами имеется аналогия в отношении оптического вращения, но не в отношении точек плавления. При 17 -ориен-тации как у тех, так и у других соединений значения положительного вращения больше, чем при 17-ориентации; более высокой точкой плавления обладают 17-эпимеры в ряду спиртов и 17 3-эпимеры в ряду эфиров. [11]
Страницы: 1