Большая подвижность - водород
Cтраница 1
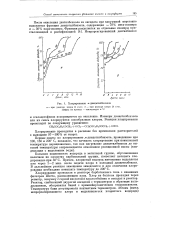 |
Хлорирование ж-диацетилбензола. [1] |
Большая подвижность водорода в метильной группе, обусловленная наличием по соседству карбонильной группы, позволяет начинать хлорирование при 50 С. Причем, хлористый водород интенсивно выделяется уже через 1 - 2 мин. В дальнейшем реакция замещения замедляется и для окончания хлорирования необходимо повышать температуру до 200 С. [2]
Большая подвижность водорода в гидроксильных группах гликолей ( и вообще многоатомных спиртов) в сравнении с одноатомными спиртами объясняется соседством ( или близостью) электроотрицательных атомов кислорода других гидроксильных групп, способностью этих атомов притягивать электроны. Однако устойчивость гликолятов тяжелых металлов обусловлена не только этим. Они имеют характер внутрикомплексных соединений. Например, состав и строение гликолята меди ( II) сложнее, чем представлено приведенной выше формулой. [3]
Это указывает на большую подвижность водорода у ( 3 - С-атома металлалкила. При пропускании изобутилена в раствор СН3Т1С13 образуется относительно устойчивый неопентилтитанхлорид. [4]
Способность ацилмалонового эфира енолизоваться определяется большой подвижностью водорода в остатке малонового эфира из-за присутствия трех сильных электроотрицательных групп. Замена метильной группы на какую-либо алкильную группу мало сказывается на протонизации водорода в метиновой группировке. Влияние алкильных заместителей определяется в основном их сте-рическими эффектами. Пространственное взаимодействие R с большой сложноэфирной группой должно дестабилизировать енол. [5]
Среди многочисленных производных антипирина особенно широко изучены различные соединения, замещенные в положении 4, так как большая подвижность водорода в этом положении пиразолонового йдра обусловливает легкость введения сюда различных заместителей. [6]
Такие реакции, которые рассматривались как маловероятные при аналогичных условиях в углеводородах, становятся преобладающими в спирте благодаря большой подвижности водорода в первичной спиртовой группе. [7]
Этот способ используют главным образом для получения гидроперекисей, содержащих один или несколько ароматических радикалов, наличие которых обеспечивает большую подвижность водорода углеводорода и облегчает окисление последнего. [8]
Для предотвращения этого процесса блокируют концевые группы линейных молекул трет. Химически такие полимеры мало устойчивы вследствие большой подвижности водорода [16], стоящего у фосфора. Термически они также не устойчивы, но пиролитическое разложение их протекает сложно и не приводит к превращению полимера в тримерные циклы. [9]
Трифенилметан получается по реакции Фриделя-Крафтса путем взаимодействия хлороформа с бензолом в присутствии А1С13 и бензальдегида с бензолом в присутствии FeCls. Присутствие в молекуле трех электроотрицательных фенильных радикалов способствует большой подвижности водорода, находящегося при центральном углеродном атоме. [10]
Как я в случае термической реакции, большая способность спиртов к окислению при действии излучений, по-видимому, связана с большей подвижностью водорода в группе СН2ОН, что облегчает перегруппировку. [11]
Как и в случае термической реакции, большая способность спиртов к окислению при действии излучений, по-видимому, связана с большей подвижностью водорода IB труппе СН2ОН, что облегчает перегруппировку. [12]
В основе синтеза, приводящего к образованию таких соединений, оказалась внутримолекулярная пиролитическая циклизация соединений, имеющих необходимые для этого структурные фрагменты. Замещенные нафталина легко циклизуются в соответствующие ацепроизводные или соединения типа феналана благодаря большой подвижности водорода в пери-положении. Пиролиз о-замещенных дифенила приводит к образованию структур типа флуорена и фенантрена, из о-замещенных бензола образуются соединения со скелетом антрацена и флуорена. Весьма успешным оказалось образование гетероциклов в две стадии, когда на первой стадии пиролиза двуххомпенентной смеси образовывалось промежуточное соединение одной из указанных структур, способное к внутримолекулярной циклизации. [13]
Хотя, как и предполагал Фрипья [116], ИК-спектры не дают однозначных доказательств подвижности или делокализации протона, все же эти данные в сочетании с более определенной информацией, предоставляемой другими методами ( ЯМР и измерения электропроводности), позволяют прийти к выводу о существовании определенного перемещения протонов при повышенных температурах. Этот вывод подтверждается также результатами, полученными при исследовании химии поверхности. Так, например, если считать правильной локализацию гидроксильных групп в решетке цеолита Y, которую мы уже рассматривали, то в таком случае способность гидроксильных групп обоих типов взаимодействовать с такими молекулами, как пиперидин и пиридин [68, 69] и кумол [119], требует определенной подвижности протонов. Кроме того, взаимодействие кумола с гидроксильными группами находится в определенной зависимости от температуры цеолита, и это тоже указывает на большую подвижность водорода на поверхности цеолитов при повышенных температурах. [14]
Натриевая соль ыетплтаурлда фенилтрпдекановой кислоты по поверхностно активным свойствам не уступает пгенону Т, полученному на основе олеиновой кислоты. Натриевые соли ме-тнлтаурпдов фенокспнонановой п феноксиундекановоп кислот значительно уступают по поверхностно активным свойствам солям метнлтауридов фенилнонановой и феннлундекановой кислот. Это объясняется тем, что введение в гидрофобную часть молекулы кислорода приводит к снижению гидрофобных свойств вещества. Замена бензола толуолом не приводит к заметному изменению свойств вещества. Сравнение продуктов, синтезированных на основе метилтаурида и таурпда, говорит в пользу применения таурида. Увеличение поверхностной активности солей таурида, по-видимому, связано с большей подвижностью водорода аминогруппы. [15]
Страницы: 1