Закон - кольрауш
Cтраница 3
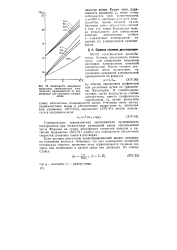 |
Зависимость кажущихся предельных эквивалентных электрических проводимостей от концентрации для некоторых электролитов. [31] |
Значение этого результата состоит в том, что закон Кольрауша можно использовать для определения констант диссоциации слабых 1 - 1-валентных электролитов и данных по электрической проводимости. [32]
Значения предельных электропроводностей ионов могут быть получены по закону Кольрауша. [33]
Этот результат имеет большое значение, так как благодаря применимости закона Кольрауша к растворам с конечными концентрациями этот закон можно использовать для определения констант диссоциации слабых электролитов по измерениям электропроводности. Следует, однако, помнить, что па рис. 19 представлены только данные для 1 1-валентных электролитов. Было установлено, что аддитивность электропролодностей одновалентных ионов наблюдается также и в случае смешанных растворителей со сравнительно высокими значениями диэлектрической: постоянной. [34]
Причиной некоторых рассмотренных выше отклонений экспериментальных значений от теоретической кривой являются неприменимость закона Кольрауша и отсутствие точного физического определения величины ct при этих концентрациях. Количественные данные, характеризующие этот эффект, отсутствуют. [35]
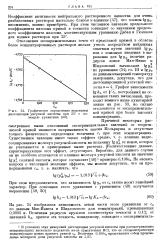 |
Графическое определение константы.. v. [36] |
Причиной некоторых рассмотренных выше отклонений экспериментальных значений от теоретической кривой являются неприменимость закона Кольрауша и отсутствие точного физического определения величины с4 при этих концентрациях. Количественные данные, характеризующие этот эффект, отсутствуют. [37]
Величина А, как было уже сказано, может быть определена по закону Кольрауша или правилу Вальдена - Писаржевского. [38]
Величина Кт, как было уже сказано, может быть определена по закону Кольрауша или правилу Вальдена - Писаржевского. [39]
В случае слабых электролитов хорошие результаты дает другой способ, основанный на применении закона Кольрауша. [40]
В 1879 г. теории электролитической диссоциации еще не существовало, поэтому современная формулировка закона Кольрауша была дана позже. [41]
В случае слабых электролитов хорошие результаты дает другой способ, основанный на применении закона Кольрауша. [42]
В двух растворителях, ацетонитриле и эпихлоргидрине, в которых был исследован целый ряд электролитов, закон Кольрауша о независимом движении ионов оказался действительным. В других растворителях, как, наприм р, альдегидах, для некоторых электролитов обнаружилось, что эквивалентные электропроводности с возрастающим разбавлением не увеличиваются, а в зависимости от природы электролита и растворителя то закономерно падают, то показывают периодический ход, проходя при этом через один или несколько максимумов или минимумов. Эти явления были объяснены химическими взаимодействиями. [43]
Как видно, приведенные в последнем столбце результаты фактически не зависят от природы катиона, что согласуется с законом Кольрауша о независимом движении ионов. [44]
Уравнение ( 57) позволяет по измеренному значению R найти величину v, по которой, в свою очередь, используя закон Кольрауша, можно рассчитать концентрацию анализируемого раствора ср. [45]
Страницы: 1 2 3 4