Закон - квантовая механика
Cтраница 1
Закон квантовой механики возводит волновокор-пускулярный дуализм частицы в ранг аксиомы. [1]
Из законов квантовой механики вытекает такое математическое следствие: возможные состояния физического объекта точно описываются представлениями его группы симметрии. [2]
Развитие законов квантовой механики достигло уже очень высокого уровня, и на современном этапе они требуют для своей интерпретации терминов вероятности. Мы не в состоянии вычислить, что может случиться в разных условиях; мы можем лишь рассчитать вероятность, с которой произойдет какое-либо событие. [3]
По законам квантовой механики электроны могут вращаться вокруг ядер не по любым орбитам. Они как бы распределяются по слоям - оболочкам. Емкость этих оболочек, максимальное число электронов в них, определяется формулой: ne2N2, где пе - число электронов, а N - номер оболочки, считая от ядра. Отсюда следует, что на первой оболочке может быть всего два электрона, на второй - восемь, на третьей - восемнадцать, на четвертой - тридцать два и так далее. [4]
Согласно законам квантовой механики электроны занимают в атоме определенные уровни энергии. При переходе с одного уровня на другой поглощается или излучается определенная энергия, равная разности энергий этих уровней. В результате столкновения электрон может получить энергию, достаточную для перехода на более высокий уровень. Однако такое состояние неустойчиво, и электрон возвращается на прежний уровень. При возврате электрон отдает энергию, равную разности энергий уровней, в виде электромагнитного излучения с частотой, зависящей от величины отдаваемой энергии. Эта частота может соответствовать видимому излучению, и тогда возникает свечение газа. Энергия, необходимая для возникновения этого явления, называемого возбуждением атома, находится в пределах от нескольких до двадцати электрон-вольт. [5]
По законам квантовой механики каждый электрон атома имеет совершенно определенное количество энергии, или каждый электрон атома может занимать только определенный энергетический уровень. [6]
По законам квантовой механики неспаренный электрон всегда стремится найти себе пару - электрон с противоположно направленным спином, а найти ее он может только в другом атоме. В результате образуются ко-валентные связи, при которых электроны двух или нескольких атомов образуют общее электронное облако. [7]
 |
Ковалентные связи, образующиеся в результате перекрывания электронных облаков. [8] |
Согласно законам квантовой механики, в прочности химической связи большую роль играет принцип максимального перекрывания электронных облаков. [9]
Согласно законам квантовой механики, эта проекция может принимать ряд дискретных значений. [10]
По законам квантовой механики, при таком узком запорном слое электрон, не обладающий энергией для преодоления потенциального барьера р - / г-перехода, может пройти через него другим путем, не затрачивая на это энергии. [11]
Согласно законам квантовой механики, не все ориентации момента по отношению к какой-нибудь оси разрешаются. [12]
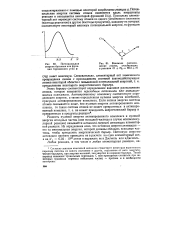 |
Взаимное расположение атомов, участвующих в реакции С1 На - НС1 Н. [13] |
Согласно законам квантовой механики существует некоторая вероятность перехода системы из одного состояния в другое, отделенное от него энергетическим барьером при энергии меньшей, чем энергия на вершине барьера. Такой переход называют туннельным переходом. С ним приходится считаться при некоторых процессах переноса небольших частиц - протона и в особенности электрона. [14]
Согласно законам квантовой механики существует некоторая вероятность перехода системы из одного состояния в другое, отделенное от него энергетическим барьером, при энергии меньшей, чем энергия на вершине барьера. Такой переход называют туннельным переходом. С ним приходится считаться при некоторых процессах переноса небольших частиц - протона и, в особенности, электрона. [15]
Страницы: 1 2 3 4