Дополнительное подтверждение
Cтраница 1
Дополнительное подтверждение того, что это не физическая адсорбция, дает тот факт, что, когда систему фторид кальция - ализарин экстрагируют безводным амиловым спиртом, в растворе не обнаруживают али-зарина. Адсорбированные на поверхности молекулы к тому же не восприимчивы к щелочным растворам. Однако при обработке разбавленной кислотой красно-фиолетовая окраска адсорбированного ализарина быстро изменяется в желтую окраску чистого ализарина. То обстоятельство, что после кислотной обработки адсорбированное вещество может быть удалено амиловым спиртом в раствор, спектр которого является спектром чистого ализарина, позволяет обнаружить вытеснение ализарина с поверхности. Ализарин, который был нагрет до промежуточной температуры ( рис. 11, кривые бис), реагирует на обработку этими реагентами так, как можно было бы ожидать для поверхности, содержащей смесь адсорбированных частиц. Вымывание спиртом приводит к частичному удалению и сопровождается изменением окраски, сходным с полученным при нагревании до более высоких температур. Таким образом, ясно, что при этих промежуточных температурах поверхность занята как физически, так и химически адсорбированным ализарином. Спектр при этих условиях должен представлять собой наложение полос поглощения, обусловленных обоими типами адсорбированных молекул. Как и в предыдущих случаях, сильно адсорбированный ализарин может быть десорбирован после кислотной обработки. Де Бур сделал вывод, что при высокотемпературной обработке адсорбированного ализарина реакция протекает на поверхности. В случае физической адсорбции молекула ализарина адсорбируется на поверхности [ структура ( А) ] путем ориентации периферийных диполей гидроксильных групп по направлению к отрицательным ионам галогенидов поверхностного слоя. Эта точка зрения дополнительно подтверждается тем фактом, что окраска ализарина, адсорбированного на фтористых барии, стронции и кальции, качественно подобна окраске, возникающей в щелочном растворе ализарина. [1]
Дополнительное подтверждение этого следует из недавних исследований скоростей роста общей кристалличности. [2]
Дополнительные подтверждения в пользу этих рисунков будут рассматриваться в разд. [3]
Дополнительное подтверждение того, что преждевременное воспламенение может вызываться отдельными частицами нагара, было найдено Мелби, Диггсом и Старгисом [32] Они вводили обычные частицы нагара, которые образуются в камере сгорания автомобильного двигателя, во всасывающее устройство одноцилиндрового двигателя. [4]
Дополнительные подтверждения того, что переходное состояние в реакциях электрофильного ароматического замещения близко по строению к а-комплексу, можно получить, изучая реакционную способность полициклических ароматических углеводородов. В этом случае различия в энергиях исходной молекулы и образующегося о-комплекса ( АЯделок) могут быть рассчитаны рядом квантовомеханических методов ( см. гл. [5]
Дополнительное подтверждение 5н2 - реакции ( 114) дано в сообщении Гоха и Онга [120], где показано, что скорости разложения 1 М раствора перекиси ди-грег-бутила в хлорзамещенных метил-бензиловых эфирах ( п-хлор, ж-хлор, 3 4-дихлор) при 110 С понижаются на 20 - 30 % при добавлении 1 моля а-метилстирола в качестве ловушки радикалов. На основании относительных скоростей разложения перекиси можно предположить, что индуцированное разложение может происходить не только в спиртах и бензиловых эфирах, но и в других растворителях. Ниже приведены количества разложившейся перекиси в некоторых растворителях через 72 ч при 110 С: декалин 43 %, трег-бутилбензол 49 %, дибензиловый эфир 50Ю / 0, метилбензиловый эфир 56 %, тг-хлортолуол 59 %, хлористый бензил 60 %, этилбензиловый эфир 62 %, бензиламин 62 %, бензаль-дегид 68 %, хлорбензол 69 %, четыреххлористый углерод 71 % ч ме-тил-ге-хлорбензиловый эфир 85 %, бензиловый спирт 85 %, а-метилбензиловый спирт 88 %, метил-3 4-дихлорбензиловый эфир 99 %, В некоторых случаях ( и частично) эти различия, вероятно, обусловлены влиянием растворителей на процесс гемолитического расщепления перекиси, а не протеканием индуцированного разложения. Например, кажется маловероятным, чтобы индуцированное разложение могло быть более существенным в хлорбензоле, чем в декалине или грег-бутилбензоле. [6]
Дополнительное подтверждение этих соображений дает работа ( 138 ], где был рассчитан температурный ход теплоемкости кристаллического метана в интервале от 5 до 90 К. [7]
Дополнительное подтверждение этого вывода можно видеть в отмеченном в работе факте, что при холоднопламенном окислении пропилена основная часть исходных веществ расходуется не в холодных пламенах, а в течение всех остальных периодов реакции, лишенных холодных пламен. Скорость же расходования исходных веществ максимальна именно в холодных пламенах. [8]
Дополнительное подтверждение этот важный вывод получил в работе [ II ], в которой проведен аналогичный анализ контуров полос первого обертона растворов галоидоводородов. Таким образом, мнение авторов [2, 7, 8] о специфической природе ШВ, препятст-вушшх вращению молекул в подобных системах, является несостоятельным. [9]
Дополнительные подтверждения были получены при длительных наблюдениях гетерологических лучевых химер. [10]
Дополнительное подтверждение согласованного механизма может быть получено из наблюдения слабой зависимости скорости присоединения от полярности растворителя. В двухстадийных вариантах ( а и б) первая стадия связана с образованием цвит-териона, заряды которого разделены тетраэдрическим атомом углерода. Так как в противоположность самому диазоалкану обмен зарядов здесь более невозможен, активированный комплекс на стадии, определяющей скорость реакции, должен был бы обладать значительно более высоким электрическим моментом. [11]
Подобное дополнительное подтверждение близости к истинным принятых расчетных параметров и условий важно в районе со сложными гидрогеологическим строением, когда всегда возникают сомнения и в правильности принятой расчетной схемы и полученных разведкой исходных данных. [12]
Дополнительное подтверждение полицентрового характера многих каталитических систем получено при изучении свойств полимеров, синтезированных на катализаторах, подвергнутых старению в отсутствие мономеров. [13]
Дополнительное подтверждение согласованного механизма может быть пожучено из наблюдения слабой зависимости скорости присоединения от полярности растворителя. В двухстадийных вариантах ( а и б) первая стадия связана с образованием цвит-териона, заряды которого разделены тетраэдрическим атомом углерода. Так как в противоположность самому диазоалкану обмен зарядов здесь более невозможен, активированный комплекс на стадии, определяющей скорость реакции, должен был бы обладать значительно более высоким электрическим моментом. [14]
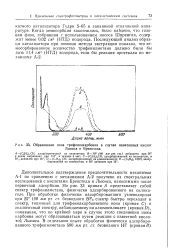 |
Образование иона трифенилкарбония в случае нанесенных кислот. [15] |
Страницы: 1 2 3 4