Подщелачивание
Cтраница 1
Подщелачивание производится аммиаком или едким натром. Концентрация рабочего раствора комплексона не должна превышать 15 г / кг. [1]
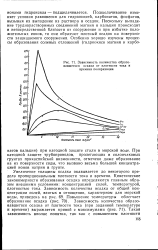 |
Зависимость количества образовавшегося осадка от плотности тока и времени поляризации. [2] |
Подщелачивание изменяет условия равновесия для гидроокисей, карбонатов, фосфатов, вызывая их выпадение из раствора в осадок. Поскольку выпадение труднорастворимых соединений магния и кальция происходит в непосредственной близости от сооружения и при избытке положительных ионов, то они образуют плотный осадок на поверхности защищаемого сооружения. [3]
Подщелачивание содержащего растворенный кислород конденсата, обеспечивающее повышение рН до 10 5, является одной из причин локализации коррозии при температуре конденсата в пределах 40 - 90 С. [4]
Подщелачивание аммиаком дает такие же результаты, так как аммиак быстро взаимодействует с формальдегидом, образуя уротропин. Реже применяются другие нейтрализующие средства, например триэтанол-амин. [5]
Подщелачивание следует проводить постепенно, при непрерывном охлаждении реакционной смеси во избежание осмоления продукта. [6]
Подщелачивание раствора способствует дальнейшему диспергированию почвенных коллоидов. Они из-за большой подвижности выщелачиваются из верхнего горизонта и на некоторой глубине под действием солей электролитов из золеобразного состояния превращаются в гели, накапливаются, что и приводит к образованию иллювиального ( солонцового) горизонта. [7]
Подщелачивание раствора сильно увеличивает прочность комплекса, так что ион редкоземельного металла не может быть выделен из комплекса даже ионами щавелевой или фтористоводородной кислот. Подкисление растворов приводит к очень сильному ослаблению комплексной связи, и при определенных значениях рН соединения редкоземельных элементов могут быть осаждены не только ионами фтора или остатком щавелевой кислоты, но даже анионами железистосинеродистой кислоты. [8]
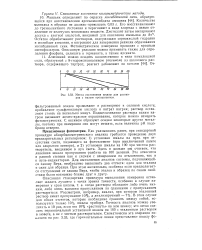 |
Метод растяжения шкалы для растворов с малым пропусканием. [9] |
Подщелачивание раствора едким натром вызывает желто-красное окрашивание, которое можно измерить фотометрически. С оксином образуют осадки некоторые другие металлы, поэтому пр и измерении они могут мешать, если величина рН подобрана неверно. [10]
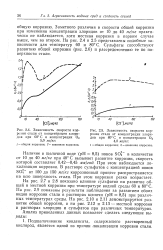 |
Зависимость скорости коррозии стали от концентрации хлоридов при 60 С и концентрации О2 5 0 мг / кг.| Зависимость скорости коррозии стали от концентрации хлоридов при 80 С и концентрации О2. [11] |
Подщелачивание конденсата, содержащего растворенный кислород, является одной из причин локализации коррозии стали. [12]
Подщелачивание раствора, которое способствует пассивации металлов, вызывает разблагораживание потенциала СОПфу в результате ускорения анодного процесса, так как ОН выступает в данном случае как агрессивный компонент раствора. Сдвиг потенциала; в этом случае значительно зависит от природы металла. Примерно на такую же величину смещается и потенвдал Ф2 - Здесь по сдвигу i потенциала трудно судить об изменении защитных свойств первич - д ной пленки на СОП. Из хода кривых ср-т видно, что время суще - j ствования первичной пленки на СОП увеличивается при введении в раствор 2 г / л щелочи в четыре раза для титана, железа и стали 2X13, а для стали 08XI8HIOT в 40 раз. Можно сказать, что подщелачивание способствует образованию на СОП более устойчивой защитной первичной пленки, которая, как и в случае с ингибитором Г-4, уменьшает скорость анодного процесса и увеличивает время до начала образования первых слоев оксида на СОП. Следует отметить, что подщелачивание раствора увеличивает скорость образования стационарной пассивной пленки на СОП железа более чем в 4 раза по сравнению с фоновым электролитом. Кроме того потенциал СОП железа при времени экспозиции I с положительное установившегося затем стационарного значения. На сталях 2X13 и 08XI8HIOT таких эффектов не обнаружено. [13]
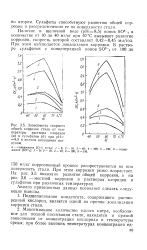 |
Зависимость скорости общей коррозии стали от температуры раствора хлоридов ( а и сульфатов ( б при рН 8 5 и полном насыщении воздухом. [14] |
Подщелачивание конденсата, содержащего растворенный кислород, является одной из причин локализации коррозии стали. [15]
Страницы: 1 2 3 4