Подщелачивание - прикатодный слой
Cтраница 1
 |
Содержание ОС покрытиях в зависимости от I - 2 25. 2 - 2 0. 3 - I. [1] |
Подщелачивание прикатодного слоя происходит быстрее и использование общепринятых буфериругощих соединений является малоэффективным. [2]
Подщелачивание прикатодного слоя может иногда служить причиной вторичного коррозионного процесса на амфотерных металлах, таких как Al, Zn, Pb, Sn. Эти металлы быстро корродируют и в кислотах и в щелочах. [3]
Пассивация цементируемого металла окислами и гидроокисями, образующимися при подщелачивании прикатодного слоя вследствие выделения водорода, затрудняет процесс цементации. [4]
На практике мы чаще встречаемся с первым случаем, когда происходит подщелачивание прикатодного слоя ( электроосаждение никеля, цинка, железа из слабокислых растворов); при этом предельное значение рН прикатодного слоя в случае образования гидратов и основных солей будет соответствовать рН образования этих труднорастворимых соединений. [5]
 |
Поляризационные зависимости выделения натрия и водорода на ртутном катоде в растворе хлорида натрия. [6] |
Реакции (3.52) и (3.53) приводят, также как и реакция выделения водорода, к подщелачиванию прикатодного слоя электролита. [7]
 |
Зависимость потенциала. [8] |
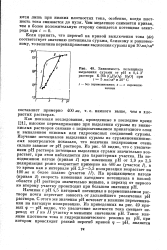
Как показали исследования, проведенные в последнее время [21], высокое перенапряжение при выделении сурьмы из виннокислых растворов связано с подщелачиванием прикатодного слоя и выпадением окисных или гидроокисных соединений сурьмы. Изучение потенциалов выделения сурьмы из сурьмяновиннокис-лых электролитов показало, что величина поляризации очень сильно зависит от рН раствора. Из рис. 48 видно, что с увеличением рН раствора потенциал выделения сурьмы значительно возрастает, при этом наблюдается два характерных участка. [9]
Для повышения электропроводности электролитов никелирования вводят соли щелочных металлов, но при высоких плотностях тока они могут быть причиной ухудшения качества никелевого осадка из-за увеличения подщелачивания прикатодного слоя. [10]
При увеличении кислотности катодный выход по току падает вследствие увеличения скорости выделения водорода, а анодный возрастает вследствие коррозии цинкового анода. При понижении кислотности выше рН 5 0 происходит подщелачивание прикатодного слоя и в связи с этим возможно выпадение у катода гидроксида цинка, который может включаться в катодный осадок, ухудшая качество покрытия. Для предотвращения подщелачивания в электролит вводят буферные добавки, например сульфат алюминия. [11]
При увеличении кислотности катодный выход по току падает вследствие увеличения скорости выделения водорода, а анодный возрастает вследствие коррозии цинкового анода. При понижении кислотности выше рН 5 0 происходит подщелачивание прикатодного слоя и в связи с этим возможно выпадение у катода гидроксида цинка, который может включаться в катодный осадок, ухудшая качество покрытия. Для предотвращения подщелачинания в электролит вводят буферные добавки, например сульфат алюминия. [12]
При увеличении кислотности катодный выход по току уменьшается вследствие выделения водорода, а анодный выход по току увеличивается за счет растворения цинка. При очень низкой кислотности ( рН 5) вследствие подщелачивания прикатодного слоя возможно образование у катода гидроокиси цинка, которая, включаясь в катодный осадок, ухудшает качество покрытия. В качестве буфери-рующей добавки в сульфатный электролит чаще всего добавляют сульфат алюминия. [13]
При цинковании с высокими плотностями тока, например при покрытии проволоки, ленты и листов, органические вещества к электролиту не добавляют. В этом случае следует избегать также введения в электролит солей натрия и калия, так как в их присутствии подщелачивание прикатодного слоя с выпадением гидроокиси цинка происходит интенсивнее. [14]
Дри дальнейшем увеличении концентрации аминоуксусной кислоты качает - К получаемых электролитических железных покрытий ухудшается. Хорошие буферные свойства этих добавок можно объяснить еще и вм, что они образуют с некоторыми металлами ( Ре, Hi) прочные ксмп - ексные соединения типа Me ( Lig) 1, благодаря чецу повышается рН гидратообразования. Значительное выделение водорода на катоде приводит быстрому подщелачиванию прикатодного слоя и выпадению гидроокиси лева. [15]
Страницы: 1 2