Закон - распределение - электрон
Cтраница 1
Закон распределения электронов по уровням энергии незначительно меняется при изменении температуры. [1]
Между законами распределения электронов по оболочкам и периодическим законом Менделеева имеется глубокая связь. Элементы нулевой группы ( инертные газы) являются элементами с полностью заполненными оболочками. Так, гелий занимает второе место в таблице Менделеева, следовательно, у него имеются два электрона, которые заполняют s - уровень в первой оболочке. Электронное строение гелия можно записать в виде Is2, где цифра 1 обозначает номер оболочки, буква s - уровень, а число электронов записывается в виде показателя степени. Начиная с атомов лития, во втором периоде идет заполнение второй оболочки, сначала s - уровня у лития и берилия и затем р-уровня - от бора до неона. Таким образом, у неона заполненными оказываются первая и вторая оболочки. [2]
 |
Уровни энергии электронов в кристалле. [3] |
Это отличие касается закона распределения электронов по энергетическим уровням. [4]
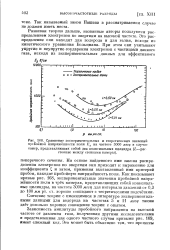 |
Сравнение экспериментальных и теоретических значений. [5] |
На основе найденного ими закона распределения электронов по энергиям они приходят к выражению для коэффициента С и затем, применяя выставленный ими критерий пробоя, находят пробойную напряженность поля. Как показывают кривые рис. 168, экспериментальные значения пробойной напряженности поля в трех камерах, представляющих собой коаксиальные цилиндры, на частоте 3000 мггц для интервала давлений от 0 3 до 100 мм рт. ст. хорошо совпадают с теоретическими подсчетами. [6]
Здесь, как и в § 44.4, п - концентрация свободных электронов, К - средняя длина свободного пробега электрона, е и т - заряд и масса покоя электрона, 1 / м - среднее значение обратной величины скорости теплового движения электронов, которое вычислено с помощью максвелловского закона распределения электронов по скоростям. [7]
Указанные факторы зависят, во-первых, от свойств эмиттера и, во-вторых, от того, каким способом сообщается электронам эмиттера дополнительная энергия. Для эмиттера с заданными свойствами закон распределения электронов по скоростям, а в некоторых случаях и концентрация электронов определяются способом возбуждения электронов. [8]
Работа [2204] содержит дальнейшее развитие той же теории. Коэффициент С вычисляется, исходя из решений, получаемых для закона распределения электронов по скоростям при высокой частоте. Таким образом, в этой работе пробойная напряженность поля рассчитывается без применения каких-либо других экспериментальных данных, кроме потенциалов возбуждения газа и эффективного поперечного сечения. Расчеты и измерения проведены для Не в широком интервале давлений ( от 0 3 до 300 мм Hg) при частоте 3000 мегагерц. [9]
Электронная температура Те и газовая температура Тг, как уже неоднократно отмечалось, являются модулями максвелловских функций распределения частиц по энергиям. Тяжелые частицы с достаточно хорошим приближением описываются максвелловской функцией распределения, в то время как закон распределения электронов нами принимается максвелловским на основании многочисленных экспериментов. Идея нахождения связи Те и Тг состоит в нахождении истинного вида функции распределения электронов по энергиям и сопоставления ее максвелловской функции распределения с модулем Те. Для нахождения функции распределения электронов необходимо составить и решить интегро-дифференци-альное уравнение Больцмана. Подробный вывод этого уравнения, его решение и нахождение связи Те и Тт даются в приложении I, здесь же рассмотрим некоторые основные моменты вывода. [10]
Понятно также, что математическая трактовка третьего случая представляет наибольшие трудности. Она возможна путем введения в закон распределения электронов по скоростям так называемых несимметричных членов, отражающих направленное движение. [11]
Химические свойства элементов связаны не с ядром атома, а с наружными электронными оболочками. Атомы с одинаковым числом электронов обладают и сходными свойствами. Периодичность свойств элементов объясняется квантовомеханическйми законами распределения электронов по электронным оболочкам атома. Ядро атома, в котором почти целиком сосредоточена масса атома, состоит из двух видов частиц: протонов и нейтронов, приблизительно одинакового веса. Как известно, атомы, имеющие одинаковый номер, но разные массовые числа, получили название изотопов. В настоящее время известно около 300 естественных изотопов и около 450 их получено искусственным путем. [12]
Первоначально было постулировано максвелловское распределение электронов плазмы по энергиям. Ход логарифмической характеристики электронного тока на зонд показал, что такое распределение действительно имеет место в большом числе случаев, а в ряде других представляет собой хорошее приближение. Но вопрос о законе распределения электронов по скоростям этим не был снят. Возникла необходимость в уточнении закона распределения, приведшая к ряду теоретических работ. Принципиально закон распределения электронов плазмы по скоростям может быть выведен из газокинетического уравнения Больцмана при условии правильного учета взаимодействий электронов с нейтральными частицами газа, с положительными и отрицательными ионами, а также между собой. [13]
Выдающийся русский ученый Д.И. Менделеев открыл универсальный закон природы, сформулированный им следующим образом Свойства простых тел ( т.е. элементов), а также формы и свойства соединений элементов находятся в периодической зависимости от величины атомных весов элементов. Это позволило создать периодическую систему элементов ( рисунок 3.27), в которой через определенные периоды повторяются сходные по свойствам элементы. Несмотря на то, что во времена Д.И. Менделеева строение атома еще не было известно, он смог предсказать свойства новых еще не открытых элементов. В последствии физики показали наличие связи между периодическим законом Менделеева и законом распределения электронов по орбитам элементов. [14]
В данном случае в качестве параметра порядка выступает число протонов ( атомный номер элемента), а управляющего параметра - масса атома. Периодический закон был сформулирован следующим образом: Свойства простых тел, а также форма и свойства соединений элементов находятся в периодической зависимости от величины атомных весов. Закон получил материальное воплощение в периодической системе элементов, в которой через определенные периоды повторяются сходные по свойствам элементы. Несмотря на то, что во времена Д. И. Менделеева строение атома еще не было известно, были предсказаны свойства, еще не открытых элементов. Впоследствии физики показали наличие связи между периодическим законом Менделеева и законом распределения электронов по орбитам элементов. [15]
Страницы: 1 2