Закон - энтропия
Cтраница 1
Закон энтропии применительно к экологическим системам. [1]
Закон энтропии позволяет предсказать направление термодинамических процессов, однако этот закон действителен лишь для таких процессов, в которых участвуют вещества, термически изолированные от окружающей среды. При этом действительно происходят только такие превращения, в которых растет энтропия. [2]
От пыли, которая ( в силу законов энтропии) обычно равномерно рассеивается по всему помещению, нетрудно избавиться, создав потенциальную яму для пылинок. Если, к примеру, установить в комнате лоток с глицерином или патокой, а пыль с помощью мощного вентилятора поддерживать в интенсивном движении, то рано или поздно все пылинки завязнут в жидкости. Пол же можно сделать слегка наклонным и время от времени заставлять его вибрировать - тогда весь мусор будет скапливаться в самом низком углу, откуда его легко убирать. [3]
Главной проблемой в термодинамике мышления является несовместимость закона энтропии для молекулярных множеств, в том числе для молекулярного аппарата мозга, и закона тождества для мышления. Вывод: молекулярное множество не способно к функции мышления. Эта антиномия, на которую до сих пор не обращали внимания, практически снимается операционной логической деятельностью сознания и, следовательно, требует фактора, способного компенсировать энтропию молекулярного аппарата мозга. [4]
В настоящей работе такой минимизацией является несовместимость законов тождества для мышления с законом энтропии для любых молекулярных множеств. [5]
 |
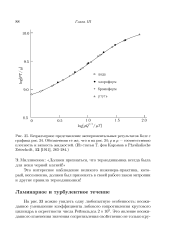
Изменение энтропии системы Src повышением температуры Т ( типовая картина. Изотермическое повышение энтропии при фазовых переходах. [6] |
Понятие энтропии лежит в основе второго начала термодинамики, которое часто называют также законом энтропии. Одна из важнейших формулировок для химической термодинамики: в изолированных термодинамических системах самопроизвольно могут протекать только такие процессы ( в том числе и химические реакции), при которых энтропия системы возрастает. [7]
Особый интерес представляет применение второго закона термодинамики в форме ( II 1.9), т.е. закона энтропии к изолированной системе. [8]
Это интересное наблюдение великого инженера-практика, который, несомненно, должен был применять в своей работе закон энтропии и другие правила термодинамики. [10]
Так, сравнительно недавно ( в ноябре 1951 г.) папа Пий XII в послании к Ватиканской Академии Наук писал: Согласно закону энтропии, открытому Рудольфом Клаузиусом, самопроизвольные природные процессы всегда связаны с уменьшением свободной энергии. В замкнутой системе это должно неизбежно вести к прекращению всех процессов макроскопического масштаба. [11]
Так, сравнительно недавно ( в ноябре 1951 г.) папа Пий XII в послании к Ватиканской Академии Наук писал: Согласно закону энтропии, открытому Рудольфом Клаузиусом, самопроизвольные природные процессы всегда связаны с уменьшением свободной энергии. В замкнутой системе это должно неизбежно вести к прекращению всех процессов макроскопического масштаба. [12]
Она означает, что для мышления, и только для него, может ие иметь места ни молекулярная, ни макроскопическая статистика, поскольку любая статистика исключает принцип тождества, который эквивалентен изъятию мышления из подчинения закону энтропии и принципу неопределенности. [13]
Рудольфом Клаузиу-сом) и заложены теоретические основы для создания паровых машин. Круговой процесс в тепловых машинах ( так называемый цикл Карно) демонстрирует закон энтропии: никакое устройство не может превратить всю тепловую энергию в кинетическую. [14]
Изложенные в предшествующих главах в точной форме понятия времени возврата молекулярного состояния - писал Смолуховский - представляют настоящий критерий пределов применимости закона энтропии. [15]
Страницы: 1 2