Закон - гей-люссак
Cтраница 1
Закон Гей-Люссака: при постоянном давлении объем образца газа пропорционален его температуре в абсолютной шкале Кельвина. [2]
Закон Гей-Люссака позволяет предсказать объем идеального газа, когда определенное его количество нагревается при постоянном давлении. [3]
Закон Гей-Люссака: объем данного количества газа при постоянном его давлении при увеличении температуры на 1 С увеличивается на 1 / 273 его объема при 0 С, и, наоборот, объем газа уменьшается на 1 / 273 его величины при 0 С в случае падения температуры на 1 С. [4]
Закон Гей-Люссака устанавливает соотношение между объемом тазов и температурой при постоянном давлении или между давлением и температурой при постоянном объеме. [5]
Закон Гей-Люссака устанавливает зависимость объема газа от температуры при его постоянной массе и давлении. [6]
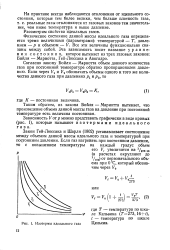 |
Изотермы идеального газа. [7] |
Закон Гей-Люссака и Шарля ( 1802) устанавливает соотношение между объемом данной массы идеального газа и температурой при постоянном давлении. [8]
Закон Гей-Люссака и Шарля ( 1802) дает соотношение между объемом данной массы идеального газа и температурой при постоянном давлении. [9]
Закон Гей-Люссака характеризует зависимость объема газа от температуры при постоянном давлении и формулируется следующим образом: при постоянном давлении изменение температуры на один градус вызывает изменение объема данного количества газа на VZTS ( более точно 11яз к) его объема при температуре 0 С. [10]
Закон Гей-Люссака устанавливает связь между объемом идеального газа и его температурой при постоянном давлении. Закон открыл в 1802 г. чисто экспериментальным путем французский химик и физик Жозеф Луи Гей-Люссак, именем которого этот закон и назван. [11]
Закон Гей-Люссака, как это видно из уравнения, утверждает, J что частное от деления объема данной массы газа на абсолютную i температуру его есть величина постоянная при данном постоянном давлении. [12]
Закон Гей-Люссака объясняет, что 0 К смещен ниже 0 С на 273 деления стоградусной шкалы. [13]
Закон Гей-Люссака можно сформулировать следующим образом: отношение объема к абсолютной температуре для данной массы газа при постоянном давлении остается постоянным. Процессы, происходящие при постоянном давлении, называются изобарными, а кривые, изображающие изобарный процесс, изобарами. Около точки t - - 273 С ( Т - 0) зависимости изображены пунктирными линиями. Это понятно, так как при низких температурах газ превращается в жидкость и законы, найденные экспериментально для газа, не работают. [14]
Закон Гей-Люссака устанавливает связь между двумя изменяющимися в процессе основными параметрами Т и v, если параметр р остается постоянным. [15]
Страницы: 1 2 3 4
