Покрытие - катализатор
Cтраница 1
Покрытие катализатора ( паллади-рованный асбест) водородистой сурьмой или водородистым мышьяком в концентрации порядка Ю-5 не оказывает отравляющего действия. Лучшие результаты - стабильное каталитическое действие при сравнении lg К в различных опытах - были получены после десяти минут. [1]
По мере увеличения степени покрытия катализатора хемосорбированным углеродом энергия активации хемосорбции метана и реакции его распада непрерывно возрастают. [2]
Селективное отравление предполагает определенные условия, а именно: 1) скорость покрытия катализатора ядом изменяется в зависимости от природы активных центров [81]; 2) количество яда, покрывающего катализатор, должно быть меньше мо но молекул яркого слоя; 3) сам яд не должен обладать никакой каталитической активностью и 4) во время избирательного отравления активные центры ведут себя так, как будто они образованы поверхностью, имеющей самую низкую теплоту активации. Конечно, отравление может быть также чисто механического характера, как это и было показано Мэкстедом [182] при гидрогенизации жидкой олеиновой кислоты в присутствии соответствующего металлического катализатора при температуре ниже температуры плавления продукта реакции - стеариновой кислоты. Накопление твердого продукта реакции на поверхности катализатора препятствует проникновению к поверхности реагентов ( водород) задолго до того, как наступает насыщение олеиновой кислоты. [3]
Превращение окиси углерода в углекислый газ сопровождается отложением кристаллов графита на железном катализаторе. Распад окиси углерода продолжается и после покрытия катализатора слоем углерода. [4]
Наиболее сложной проблемой, возникающей в процессе каталитического сжигания, является постепенная дезактивация или отравление катализатора при длительном сроке службы или при неожиданном появлении ядов в газовом потоке. Дезактивация обусловлена либо химическим взаимодействием газов с катализатором, либо покрытием катализатора слоем дезактивирующего вещества. [5]
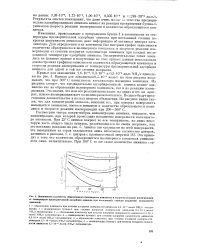 |
Зависимость количества образованного полимерного комплекса и скорости реакции изомеризации от температуры предварительной адсорбции аммиака при постоянной степени покрытия поверхности аммиаком. [6] |
Изменения, происходящие в превращении бутена-1 в зависимости от температуры предварительной адсорбции аммиака при постоянной степени покрытия цоверхности аммиаком, дают информацию об активных центрах катализатора. Для определения этих изменений был построен график зависимости количества образующегося полимерного комплекса и скорости реакции изомеризации от степени покрытия катализатора аммиаком при каждой исследованной температуре адсорбции аммиака. Экспериментальные точки ложились на плавные кривые и полученные из этих кривых данные использовали для построения графиков зависимости количества образующегося комплекса и скорости реакции изомеризации от температуры предварительной адсорбции аммиака для одной и той же степени покрытия. [7]
Срок службы катализатора в промышленном реакторе - один из параметров, которые особенно трудно оценить в лабораторных реакторах. Это объясняется тем, что снижение каталитической активности вызывается рядом причин, которые обычно недостаточно выяснены. Покрытие катализатора продуктами уплотнения органических соединений ( закоксовывание), его отравление, рекристаллизация, закупорка пор и другие процессы дезактивации могут происходить по-разному в лабораторном реакторе и в разных частях промышленного реактора. [8]
Можно предположить, что в случае более ковалентного характера связи атома с поверхностью приемлем метод Стоуна и Хабера [9], так как кулоновское взаимодействие уменьшается и существенную роль может играть влияние поля лиганда. Если этот ион снова превращается в Сг3 ( d3) за счет присоединения электрона от соседних ионов хрома в объеме, то влияние стабилизации в октаэдрическом поле для ковалентной связи может уравновешиваться уменьшением ионного притяжения. Таким образом, мы снова пришли к выводу, что этот процесс, который более вероятен для катализаторов МС, обусловливает большую степень покрытия катализатора типа MCL слабо хемосорбированным кислородом. Предполагаемое объяснение не учитывает роли дефектов, существующих на поверхности. Их значение выявляется при рассмотрении чистых окислов переходных металлов, а исследования на N10 и MgO - NiO [ 10J четко показали различие, наблюдаемое для разбавленных и концентрированных твердых растворов. В последнем случае влияние изменения концентрации может перекрываться влиянием изменения структуры поверхностных дефектов. По нашему мнению, структура поверхности чистых окислов переходных металлов может быть такова, что вероятно наличие нескольких типов дефектов, которые оказывают влияние на прочность связи кислорода с поверхностью, допуская высокую подвижность хемосорбированного кислорода. Для этого требуется покрытие большей части поверхности частиц MgO хромитом при более высоком содержании хрома. Активность МС 1 в реакции разложения N20 выше, поэтому, по-видимому, небольшие участки хромита, присутствующие в МС 1, более активны, возможно, вследствие большей неупорядоченности. [9]
Можно предположить, что в случае более ковалентного характера связи атома с поверхностью приемлем метод Стоуна и Хабера [9], так как кулоновское взаимодействие уменьшается и существенную роль может играть влияние поля лиганда. Если этот ион снова превращается в Сг3 ( d3) за счет присоединения электрона от соседних ионов хрома в объеме, то влияние стабилизации в октаэдрическом поле для ковалентной связи может уравновешиваться уменьшением ионного притяжения. Таким образом, мы снова пришли к выводу, что этот процесс, который более вероятен для катализаторов МС, обусловливает большую степень покрытия катализатора типа MCL слабо хемосорбированным кислородом. Предполагаемое объяснение не учитывает роли дефектов, существующих на поверхности. Их значение выявляется при рассмотрении чистых окислов переходных металлов, а исследования на N10 и MgO - NiO [ 10J четко показали различие, наблюдаемое для разбавленных и концентрированных твердых растворов. В последнем случае влияние изменения концентрации может перекрываться влиянием изменения структуры поверхностных дефектов. По нашему мнению, структура поверхности чистых окислов переходных металлов может быть такова, что вероятно наличие нескольких типов дефектов, которые оказывают влияние на прочность связи кислорода с поверхностью, допуская высокую подвижность хемосорбированного кислорода. Для этого требуется покрытие большей части поверхности частиц MgO хромитом при более высоком содержании хрома. Активность МС 1 в реакции разложения N20 выше, поэтому, по-видимому, небольшие участки хромита, присутствующие в МС 1, более активны, возможно, вследствие большей неупорядоченности. [10]
Интересно сопоставить результаты, полученные А. Ф. Плата и М. И. Батуевым 85 по диспропорционированию водорода в циклопентене, с результатами, полученными А. В. Фростом 89 - 90 а также Томасом и сотрудниками. Как американские авторы, так и фрост всегда указывают на полимеризацию как на основную реакцию олефинов ( циклических и алифатических) и на последующее гидрирование олефинов. На основании данных А. Ф. Плата и М. И. Батуева эти представления следует уточнить. Главной реакцией в ряде случаев каталитических превращений углеводородов и, вероятно, в случае каталитического крекинга является реакция диспропорционирования водорода, в результате чего из олефинов образуются, с одной стороны, парафины ( или циклопарафины), а, с другой, диены. Именно последние в условиях опыта полимеризуются и притом гораздо легче, чем исходные моноолефины, что ведет к покрытию катализатора инактивирующей пленкой. Циклопентадиен ввиду его устойчивости и сравнительной легкости, с которой он может быть идентифицирован, удалось обнаружить. Другие диены также, вероятно, образуются, но обнаружить их труднее. [11]
Страницы: 1