Сильное положительное поле
Cтраница 1
Сильное положительное поле этих ионов выбивает электроны из катода, и в результате возникают возбужденные нейтральные молекулы, переходящие в преддиссоциированное состояние до того, как они ударятся о стенку и освободят вторичные электроны. Счетчик Гейгера-Мюллера, наполненный такой смесью, называется бы - стрым счетчиком и не § нуждается во внешних § электронных цепях для погашения разряда. [1]
Ввиду очень сильного положительного поля Р5 (2.08) в фосфорноки-слородном каркасе возможно образование очень прочных кислородных связей внутри тетраэдра и ослабление межструктурных связей, что объясняет легкоплавкость этого соединения. [2]
Тиосульфат-ионы стабилизируются в сильном положительном поле катионов щелочных металлов. [3]
Если в слабо легированном электронном полупроводнике осуществляется условие I Po / ( bna ра), то при наложении сильного положительного поля происходит обеднение приконтактной области неосновными носителями. Это явление носит название эксклюзии носителей заряда. [4]
Приведенные данные свидетельствуют о трудной отщепля-емости от молекул кислоты их протонов и значительно более легком растяжении и разрыве связей между составляющими их группами NO2 и ОН, о сильном положительном поле групп NO2 и их способности с большой энергией взаимодействовать с частицами с отрицательным полем, о значительном отрицательном поле групп ОН и их способности притягиваться и взаимодействовать с частицами с положительным полем. Это значит, что в условиях положительного электрического поля анода молекулы азотной кислоты могут поляризоваться с концентрацией положительного заряда у групп NO2 и отрицательного заряда у групп ОН и с значительным растяжением и ослаблением связей между этими группами. Группами ОН они могут притягиваться и взаимодействовать с положительно заряженной поверхностью анода, с ионами металла этой поверхности и поверхностного окисла металла, а группами NO2 взаимодействовать с ионами кислорода названного окисла. Указанные взаимодействия групп NO2 и ОН, значительно усиленные поляризацией молекул кислоты, еще более ослабляют связи между этими группами. [5]
Сильное положительное поле может наблюдаться непосредственно под грозовым облаком, сопровождаемым сильным дождем, хотя предразрядное поле в этом случае, как правило, отрицательно. После каждого разряда наблюдается процесс восстановления со временем релаксации примерно 7 с. В случае когда в облаке происходят разряды внутренними молниями, каждый такой внутренний разряд нарушает биполярное распределение заряда, но затем электрический дипольный момент все равно восстанавливается. [6]
Мюллер ( E. W. Miiller, Pennsylvania State University): По-видимому, некоторые новейшие методы эмиссионной микроскопии могли бы быть использованы при изучении адсорбции, например адсорбции азота на вольфраме. Постепенная десорбция путем испарения или наложения сильного положительного поля [6] позволяет получить дополнительные сведения. Оказывается, что плоскость ( 001) на вольфраме развита не настолько хорошо, чтобы ее можно было использовать для выводов, сделанных в работе Брока. Метод цветной фотографии [8] непосредственно указывает на локализацию адсорбированных зеленых атомов W, О или N на желтом вольфрамовом субстрате. В случае азота применение этого метода, вероятно, ограничено малыми степенями заполнения, при которых атомы прочно связываются в углублениях вдоль уступов решетки. [7]
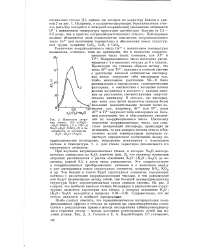 |
Изменение энтропии стекол ( 18 -. r Na20 iK2O - 82Si02 ( 7 и ( 28 - 1 / Na20 -. / K20 - 72Si02 ( 2 в зависимости от отношения К2О. ( K20 Na2O. [8] |
Координационное число последних увеличивается с 4 в основных стеклах до 6 в кислых. Происходит это главным образом потому, что ионы А13 или Ti4, находясь в окисной системе с достаточно высокой активностью кислородных ионов, окружают себя кислородом так, чтобы межатомное расстояние Me-О было минимальным и определялось геометрическими факторами, в соответствии с которыми катион должен находиться в контакте с каждым анионом на расстоянии, соответствующем энергетическому минимуму. В стеклах, где кислородные ионы уже почти полностью связаны более сильными положительными полями таких ка-тионов, как, например, Si4 или В3, ионы А13 и Ti4 окружают себя кислородом на боль-шем расстоянии, что и обусловливает увеличение их координационного числа. [9]
 |
Механизм дегидратации и исследующей дезактивации диоксида кремния при температурах свыше 400 С ( схема. [10] |
В отличие от диоксида кремния активность оксида алюминия повышается при нагревании вплоть до 1000 С. Это служит убедительным доказательством, что активными центрами на поверхности оксида алюминия являются не гидроксильные группы. В действительности, как можно судить по характеристикам удерживания, при хроматографировании на оксиде алюминия проявляются три типа взаимодействий растворенного вещества с адсорбентом. В первом типе адсорбаты с легко поляризующимися электронами ( основания Льюиса) взаимодействуют с очень сильными положительными полями вокруг ионов А13 на поверхности оксида алюминия. Взаимодействия второго типа приводят к преимущественному удерживанию кислых растворенных веществ, по-видимому, в результате образования донор-но-акцепторных связей между протонами и основными центрами ( О2 - - ионами) на поверхности оксида алюминия. И, наконец, некоторые соединения ароматического ряда, очевидно, удерживаются в результате взаимодействий, связанных с переносом заряда, возможно из-за переноса электрона к положительно заряженным А13 - центрам. Кажется-совершенно естественным, что когда два растворенных вещества отличаются главным образом своей электронной структурой, то из адсорбентов наиболее предпочтителен в этом случае оксид алюминия. Так, он превосходит диоксид кремния по разделению ароматических ил, олефиновых углеводородов. [11]
Страницы: 1