Политерма
Cтраница 2
Политерма указанной системы ( рис. 25.2) показывает, что точка / j с повышением температуры перемещается. [16]
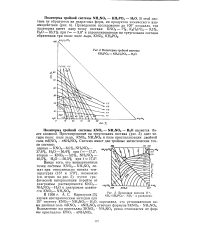 |
Политерма тройной системы КН2РО4 - NH4H. PO - Н2О.| Безводная система К, NH4 [ H2PO4 -, NO3 - в расплавах. [17] |
Политерма тройной системы KNO3 - NH4NO3 - Н2О является более сложной. [18]
Политерма данной системы имеет сложный вид. Между компонентами в водном растворе происходит взаимный обмен по уравнению NH4NO3 KH2PO4 NH4H2PO4 KNO3c образованием внутри политермы самостоятельного поля. [19]
Политерма данной системы является сложной. [20]
 |
Изотермы растворимости тройной системы при различных температурах. Состав системы иаображеа ио методу Розебома ( а и ио методу Скрейнемакерса ( б. [21] |
Политерма растворимости тройной системы является объемной фигурой и на плоскости может быть изображена в виде проекции. По этой причине политермы растворимости строятся редко. [22]
Структурная политерма пятерной системы Na, NH4 C1, НСОз, ОН Н2О от - 30 до 60 и ее применение в теории содо-нашатыр-ного процесса. [23]
Политерму на плоскости можно изобразить как совокупность ряда изотерм, подобно тому, как на географических картах местность изображают горизонталями равных высот. Если на изотермах каждая ветвь кривой растворимости соответствует определенной твердой фазе, то на политерме каждая ветвь кривой растворимости соответствует растворам, насыщенным двумя твердыми фазами. Одной твердой фазе соответствует уже не кривая растворимости, а ограниченная часть поверхности кристаллизации политермы. [24]
Линии политермы отвечают моновариантному состоянию равновесия, в данном случае равновесию между двумя твердыми фазами и раствором. [25]
Рассмотрение политермы до температуры плавления солей чаще всего неоправдано и не позволяет изобразить политерму в удобном масштабе. [26]
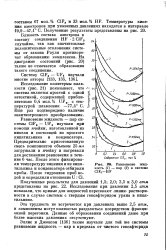 |
О. Равновесие жидкость ( 1 - пар ( 2 в системе C1F3 - HF. [27] |
Исследование политермы плавкости ( рис. 21) показывает, что система является простой с одной эвтектикой, содержащей приблизительно 0 4 мол. [28]
Элементами политермы тройной системы являются: поверхности-поля кристаллизации, линии и точки. [29]
Анализ политермы растворимости солей в этой системе показывает, что практически невозможно с приемлемым технологическим выходом отделить полезные калийно-магниевые минералы от галита одностадийным растворением руды в воде или оборотных щелоках. Даже в простейшем случае, когда в полиминеральной руде содержатся только легкорастворимые калийные минералы ( каинит, шенит, сильвин, карналлит), образующиеся при растворении руды щелока всегда насыщены хлоридом натрия и выделение из них чистых калийных солей затруднено. [30]
Страницы: 1 2 3 4 5