Закономерность - изменение - каталитическая активность
Cтраница 1
Закономерности изменения каталитической активности в дегидрировании тетралина [347, 414] аналогичны дегидрированию циклогексана. [1]
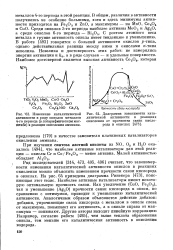
Ряд исследователей [314, 473, 495, 496] считает, что закономерности изменения каталитической активности окислов в реакциях окисления можно объяснить изменением прочности связи кислорода в окислах. На рис. 64 приведена диаграмма Ринекера [473], поясняющая этот тезис. Наиболее активные катализаторы имеют некоторую оптимальную прочность связи. Как увеличение ( CuO, Fe203), так и уменьшение ( Ag20) прочности связи кислорода в окиси, по сравнению с оптимумом, приводит к уменьшению каталитической активности. Аналогичным образом объясняется действие добавок: добавки, упрочняющие связь кислорода с металлом в окисле слева от максимума, повышают его активность, а в окисле справа от максимума - понижают. Другие авторы находят линейную корреляцию Например, согласно работе [495], чем выше теплота образования окисла, тем меньше его каталитическая активность в окислении водорода. [3]
Другим интересным результатом наших исследований является установление закономерности изменения каталитической активности никелевых катализаторов с изменением параметра решетки никеля. Изменение скорости гидрирования непредельного соединения и электроокисления водорода антибатно, и изменение энергии активации миграции водорода и электроокисления его симбатно изменению параметра решетки никеля. Во всех случаях максимумы и минимумы кривых изменения этих свойств соответствуют минимальному значению параметра решетки. [4]
В работе Даудена, Маккензи и Трепнела [54] были установлены закономерности изменения каталитической активности в реакции изотопного обмена водорода с дейтерием на окислах переходных металлов четвертого периода. Эти данные можно считать наиболее надежными, поскольку каталитическая активность относилась к единице поверхности и процесс протекал в кинетическом режиме. Дауден исследовал обмен на тринадцати окислах элементов IV периода при температурах от - 195 до 20 С и давлении 10 - 50 торр. [5]
В работе Даудена, Маккензи и Трепнела [61] были установлены закономерности изменения каталитической активности в реакции изотопного обмена водорода с дейтерием на окислах переходных металлов первого большого периода. В ряду этих окислов было обнаружено два пика активности. По-видимому, тот же самый тип активности проявляется в реакциях диспропор-ционирования циклогексенов [62] и гидрирования этилена [63] на окисных катализаторах. [6]
Теория кристаллического поля удобна для химиков, так как она связывает каталитическую активность непосредственно с химическими свойствами катализаторов. Эта теория удовлетворительно объясняет сходство закономерностей изменения каталитической активности соединений переходных металлов, наблюдавшееся в ряде случаев в гомогенном и гетерогенном катализах. Например, в окислительно-восстановительных реакциях в растворах относительные каталитические активности ионов Со2 / Со3, Ni2 / Ni3 и Мн2 / Мп3 приблизительно такие же, как и в реакции окисления С2Н4 на твердых окислах Со, Ni и Мп. Ионы Мп2 и Fe3, свободные или в составе комплексов, ведут себя обычно так же, как ионы непереходных металлов. [7]
Полимеризация ацетальдегида была изучена [652] на большом числе окисных катализаторов. Механизм ее, по-видимому, также координационно-ионный или кислотный по Льюису, однако закономерности изменения каталитической активности отличаются от соответствующих закономерностей для полимеризации олефинов. Несколько менее активны В203, Р205, MgO, Th02, алюмосиликат. [8]
Изомеризация циклопарафинов в олефины протекает, по-видимому, по такому же механизму как изомеризация олефинов - через образование иона карбония. Индивидуальные окислы ( А1203, Si02), имеющие малую протонную кислотность, каталитически неактивны. Закономерности изменения каталитической активности в реакции изомеризации циклогексана в метилциклопентан ( как и в крекинге циклогексана) также объясняются автором работы [422] с точки зрения положений карбониево-ионной теории. [9]
Глубокое окисление пентана, 2-пентена, 1-пентина, 2-метил-бутана, 2 3-диметилбутана, гексана, циклогексаиа и бензола было изучено одними и теми же исследователями [539] проточно-хрома-тографическим методом. На рис. 70 сопоставлены значения каталитической активности окислов металлов 4-го периода для глубокого окисления перечисленных углеводородов. В качестве меры каталитической активности принята температура 80 % - ного превращения, так как удельные поверхности их изменялись не очень сильно. Температурный интервал окисления разных углеводородов ( 200 - 600 С) остается приблизительно одним и тем же. Как видно из рис. 70, одинаковыми являются и закономерности изменения каталитической активности. [10]
Страницы: 1