Полнота - связывание
Cтраница 1
Полнота связывания конденсатором водяного пара находится в зависимости от его температуры: чем выше температура конденсатора, тем большее количество молекул пара отражается от его поверхности и попадает вновь в окружающее пространство, увеличивая тем самым давление пара в конденсаторе и снижая скорость высушивания. Следовательно, оптимальной является такая температура конденсатора, при которой происходит полное связывание всех молекул водяного пара, достигающих охлажденной поверхности, т.е. когда коэффициент аккомодации равен единице. По разным источникам, эти условия наступают при температуре от - 60 до - 100 С. [1]
Полнота связывания окиси кальция в более сложные соединения не всегда определяется лишь температурным уровнем в топке, иногда определяющим являются и стехиометрические соотношения между окисью кальция и другими минералами в неорганической части топлива и коэффициент шлакоулавливания в топке. [2]
Полнота связывания галогенокислоты металла в тройной комплекс зависит от ряда факторов, и прежде всего от кислотности раствора. В системе М - Am-Hal образуется два труднорастворимых соединения: Am - М - Hal и соль основного красителя AmHal. Галогенокислота металла Hm B [ M Halm ], как комплексная кислота, должна быть сильнее, чем соответствующая ей галогеноводородная кислота. [3]
По-видимому, полнота связывания С2Н2 определяется суммарным действием нескольких факторов: скорости реакции образования Cu2C2, растворимости С2Н2 в реактиве и стойкости медно-аммиачного комплекса, по-разному зависящих от температуры. Возможно, что при 0 С действие последних двух факторов является преобладающим. [4]
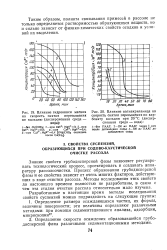 |
Влияние гидроокиси магния.| Влияние полиакриламида на скорость снятия пересыщения по карбонату кальция при 20 С ( дисперсионная среда - вода. [5] |
Таким образом, полнота связывания примесей в рассоле не только определяется растворимостью образующихся веществ, но и сильно зависит от физико-химических свойств осадков и условий их выделения. [6]
Довольно часто для полноты связывания ионов металла в комплекс реакции комплексообразования проводят в слабо щелочной среде. Однако в сильно щелочных средах комплексообразование обычно не проводят, чтобы избежать гидролиз ионов металлов и образование гидроксидов металлов. [7]
Значительно влияет на полноту связывания формальдегида способ введения карбамида в реакцию. При введении одного и того же количества карбамида в три приема содержание свободного формальдегида в смоле примерно в 2 раза меньше, чем при одновременном введении всей порции карбамида. Каждая последующая порция карбамида способствует сдвигу установившегося равновесия в сторону образования мочевиноформальдегидных соединений. [8]
Один из важных факторов, влияющих на полноту связывания фенола с формальдегидом - продолжительность конденсации смол при температуре кипения реакционной смеси, с увеличением которой за счет более глубокого процесса конденсации резко снижается содержание свободного фенола в готовой смоле. В то же время вязкость готовой смолы увеличивается, что может оказать отрицательное влияние на срок ее хранения. [9]
При применении реактивов, являющихся слабыми кислотами, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реактивом индикаторных свойств. Всегда при проведении таких реакций есть интервал рН, в котором происходит достаточно полное связывание определяемого иона в комплекс, а изменения окраски самого реактива еще не происходит. [10]
При применении реагентов, являющихся слабыми кислотами, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реагентом индикаторных свойств. Всегда имеется интервал рН, в котором происходит достаточно полное связывание определяемого иона в комплекс, а окраска самого реагента еще не изменяется. [11]
Предположение, высказанное в работе [5], что вследствие экзотермичности реакции образования CU2C2 полнота связывания С2Н2 существенно возрастает с понижением температуры, нельзя считать достаточно обоснованным. [12]
При применении реактивов, являющихся слабыми кислотами, как указывалось в предыдущем разделе, полнота связывания определяемого иона в комплекс возрастает с увеличением рН раствора. Однако при этом необходимо учитывать возможность проявления реактивом индикаторных свойств. Регулировка кислотности раствора при использовании р еакти BOB, о б л а д а ю щи х индикаторными свойствами, имеет первостепенное значение. [13]
Практическая полнота выделения следов элементов из их чрезвычайно разбавленных растворов зависит от двух причин: от полноты связывания элементов в соосаждаемые соединения и полноты извлечения этих соединений из раствора в твердую фазу. [14]
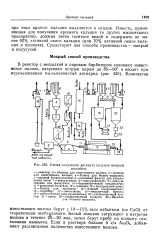 |
Схема получения арсенита кальция мокрым способом. [15] |
Страницы: 1 2 3