Положение - предел - воспламенение
Cтраница 1
Положение предела воспламенения в данном случае нельзя было предвычислить, так как не был известен тепловой эффект реакции. [1]
Далее теория была применена к предсказанию положения предела воспламенения там, где он экспериментально ранее не наблюдался. Удалось предсказать тепловое воспламенение закиси азота - явление, ранее совершенно неизвестное. Экспериментально определенный Зельдовичем и Яковлевым [8] предел воспламенения хорошо сошелся с предвычисленным теоретически. [2]
Изложенная теория позволяет для реакций с известной кинетикой предвычислять положение предела воспламенения. Эта возможность была как нами, так и рядом других исследователей в СССР и за рубежом применена к решению разнообразных задач. Прежде всего теория была проверена нами [5] на нескольких реакциях, для которых кинетика, предел воспламенения и другие необходимые для расчета величины были хорошо известны из литературы и относительно которых уже и ранее были веские основания предполагать, что взрыв имеет тепловую природу. Первые три реакции имеют простую мономолекулярную, четвертая - довольно сложную автокаталитическую кинетику. В трех случаях расчет дал результаты, очень хорошо сходящиеся с экспериментом; для этилазида получилось некоторое расхождение, причина которого неясна. [3]
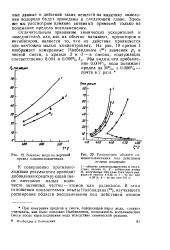 |
Влияние иода на верхний предел самовоспламенения.| Расширение области самовоспламенения под действием атомов водорода. [4] |
Здесь же мы рассмотрим влияние активных примесей только на положение предела воспламенения. [5]
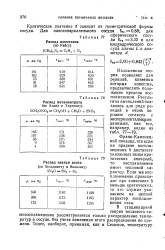 |
Распад закиси азота ( по Зельдовичу и Яковлеву 2N20 2Na - Ь 02. [6] |
Изложенная теория позволяет для редакций, кинетика которых известна, предвычислять положение предела воспламенения. [7]
Из этого следует, что для определения констант скоростей превращения какого-либо радикала по положению предела воспламенения и по его смещению необходимо изучать такие системы, в которых реакция, определяющая эффективную скорость разветвления, происходила бы при непосредственном участии данного радикала. [8]
Это выражение использовано [45] для вычисления положения пределов воспламенения смеси 2Н2 - 02 при различных температурах. Таким образом, если значения Q и Е достаточно велики, то период индукции составляет малую долю общей продолжительности процесса, и к моменту его окончания успевает разложиться не более ( 0 1 - 1) % исходных веществ. На практике это условие реализуется достаточно часто, но не всегда. [9]
Эти процессы приводят к увеличению числа активных центров, что изменяет положение пределов воспламенения, хотя оно сохраняет тепловую природу. При медленном взаимодействии, а возможно, и при реакции в пламени роль разветвлений несущественна. [10]
Авторы ссылаются, однако, на экспериментальные данные, которые подтверждают наличие процесса разветвления цепей в ходе окислительной реакции, приводящей к верхнетемпературному воспламенению. Отсюда Льюис и Эльбе приходят к выводу, что скорость реакции сама по себе еще не определяет положения предела воспламенения. Такой вывод, понятно, не может быть согласован с представлением о чисто тепловой причине взрыва, поскольку в этом случае углеводородо-кислород-ная смесь того состава, при котором реакция обладает наибольшей скоростью, должна была бы обладать наименьшей температурой воспламенения. [11]
Дальнейшее подтверждение гипотезы о роли разветвлений можно видеть в том, что полученное в таких предположениях выражение позволяет наиболее точно описать результаты по изучению медленного окисления метана. Хотя это доказательство не может считаться решающим, мы тем не менее будем принимать, что при высоких температурах протекает реакция разветвления цепей, определяющая в основном положение предела воспламенения, хотя мы и не будем отрицать возможности одновременного существования вторичного теплового эффекта, несколько смещающего предел в сторону низких давлений. [12]
Страницы: 1