Положение - фенильная группа
Cтраница 1
Положение фенильной группы не было вполне выяснено, но считали вероятным, что продуктом была 10-фенилстеариновая кислота. [1]
Если установлено положение фенильной группы ( экзо или эндо, ср. LXIII и LXIV соответственно) в одном из этих двух ( оптически активных) кетонов, то можно сделать заключение об абсолютной конфигурации ферроценовой хиральной части, ( R) p или ( S) F, из определенной ранее абсолютной конфигурации хирального центра ( S) c в рассмотренном здесь примере. [2]
 |
Эфиры ментола. [3] |
Из этой таблицы видно, что положение фенильной группы в оптически активном комплексе оказывает очень сильное влияние на молекулярное вращение соответствующего эфира. [4]
Этот результат является решающим для выбора положения фенильной группы в системе камфана, как это было указано в теоретической части. При перегонке масла, не растворившегося в щелочи, большая часть его не перегналась до 160 С ( 17 мм); очевидно, по крайней мере в главной части, это уже не 4-фенил-камфан, а какой-то не содержащий азота продукт взаимодействия 4-фенилкамфана с азотной кислотой. [5]
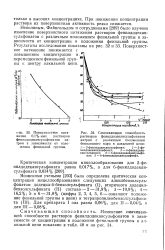 |
Смачивающая способность растворов фенилдодекансульфонатов натрия с различным положением бензольного ядра в алкильной цепи. [6] |
Поверхностное натя-жевие 0 1 % - ных растворов фенилдодекансульфонатов натрия в зависимости от положения фенильной группы. [7]
Неволиным, Файнгольдом и сотрудниками [209] было изучено изменение поверхностного натяжения растворов фенилдодекан-сульфонатов с различным положением фенильной группы в зависимости от концентрации и положения фенильной группы. Поверхностное натяжение понижается с повышением концентрации и перемещением фенильной группы к центру алкильной цепи. [8]
Александер и Чарлзби [45, 46] нашли, что сополимер изобути-лена с 20 % стирола требует в среднем 32 эв для одного разрыва главной цепи по сравнению с 17 - 20 эв для полиизобути-лена. Здесь положение фенильных групп по отношению костальным частям молекулы точно не определено. Дальнейшие доказательства получены теми же авторами при измерении дозы реакторного излучения, необходимой для создания сплошной пространственной сетки в ряду замещенных додеканов. Образование сплошной сетки с желатинированием и возникновением неплавкости наступает тогда, когда одна поперечная связь приходится на средневесовую молекулу. Для самого додекана требуется 27 реакторных единиц. Присоединение насыщенной полициклической водородной группы ( группы 2 -декалила) вблизи середины цепи несколько увеличивает дозу, необходимую для возникновения неплавкости. Данные табл. 6 подтверждают существование заметного стабилизирующего эффекта. Этот эффект не может быть обусловлен в основном пространственными причинами, так как он значительно больше, чем эффект, создаваемый насыщенной 2 -дека-лил - группой, имеющей ту же величину. Он, по-видимому, спадает достаточно быстро с увеличением расстояния вдоль цепи, а поэтому нафтильные группы, расположенные в конце цепи, менее эффективны, чем занимающие положение ближе к центру. Эти результаты достаточно доказательны лишь в соединении с другими данными; взятые сами по себе, они не приводят к однозначному заключению, так как могут быть объяснены на основании предположения, что ароматические группы ускоряют деструкцию, а не задерживают сшивание. [9]
Оно позволяет заключить, что для комплекса Т1 ( 1), радиус которого 1 47 А, значение Ямакс было бы равно 450 ммк; это совпадает со вторым максимумом поглощения самого дитизона, так что при определении Т1 этим способом незакомплексованный дитизон мог бы оказывать серьезные помехи. Введение метальных радикалов в п, n - положения фенильных групп дитизона смещает максимумы поглощения примерно на 10 ммк в сторону более длинных волн. Замена фенильных остатков нафтильными также приводит к смещению максимумов в длинноволновую область. [10]
Изучено электроокисление некоторых простых 1 2 3 4-тетра-гидроизохинолинфенолов [139] на Pt, графитовом и Hg-анодах ( катод свинцовый) в водных растворах Na2B4O7 и НС1 и в аце-тонитрильных растворах на фоне ( CaHs NClCU в ячейке с пористой стеклянной диафрагмой. В результате исследований установлено, что идет образование димерных продуктов. Выходы конечных продуктов зависят от рН, положения фенильной группы в ароматическом кольце и положении N-атома в гетероцик-ле, наиболее высокие выходы продуктов получаются на графитовом аноде в ацетонитрильном растворе при электролизе Na-солей исследуемых фенолов. [11]
В связи с развитием производства линейных алкилбензолсульфонатов, легко биологически разрушаемых в сточных водах, были проведены исследования действия этих веществ на рыб. Установлено, что они действуют на рыб в большей степени, чем тетрапропиленбензолсульфонат. Это действие зависит от длины алкильной цепи и положения фенильной группы. [12]
Страницы: 1