Положение - метоксильная группа
Cтраница 1
Положение метоксильных групп в молекуле метилцеллюлозы может быть достаточно точно определено при помощи методов, применяемых для определения положения гидроксильных групп в не полностью замещенных эфи-рах целлюлозы ( гл. [1]
В данном случае должен выясниться вопрос, является ли положение метоксильной группы в акрихине наиболее благоприятным с точки зрения противомалярийной активности и как будет изменяться активность при изменении места, занимаемого метоксильной группой. [2]
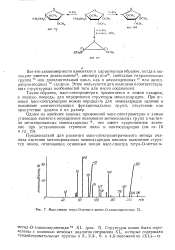 |
Масс-спектр тетра - О-метил-а - метил - О-глюкопиранозида XL. [3] |
Одним из наиболее важных применений масс-спектрометрии в химии углеводов является определение положения метоксильных групп в частично метилированных моносахаридах 7S, что имеет существенное значение при установлении строения поли - и олигосахаридов ( см. гл. [4]
Очень интересную группу веществ образуют стильбены, родственные флавоноидным соединениям, главным образом по положению гидроксильных и метоксильных групп. Они и встречаются вместе, однако преимущественно в древесине и корнях, а не в других тканях побегов. [5]
Степень метилирования изучаемого метилированного сахара определяется на основании хроматографических и аналитических данных. Дальнейшее определение строения сводится к установлению положения метоксильных групп в молекуле. [6]
Строение болдина установлено при помощи стандартных способов, разработанных для исследования неполностью алкилированных представителей этого ряда. Определив положение, занимаемое атомами кислорода, путем превращения алкалоида в глауцин, Варнат75 пытался установить положение метоксильных групп при помощи окисления. Если бы обе защищенные гидроксильные группы находились в одном ядре, то они должны были бы сохраниться в бэнзолдикарбоновой или трикарбоновой кислоте; однако в процессе окисления, повидимому, произошло разрушение обоих концевых ядер, так как получилась только щавелевая кислота. [7]
Аналогичным примером является различие в поглощении дибензантроном и 16 17-ди-метоксидибензантроном. Пространственные препятствия, вызванные наличием атомов водорода в положениях 16 и 17 в молекуле ди-бензантрона, сильно увеличиваются с введением в эти положения метоксильных групп, как, например, в Каледоновом нефритово-зе-леном. Поскольку добавочная энергия, необходимая для достижения планарности конфигурации молекулы, должна быть вычтена из энергии резонанса, максимум поглощения диметоксисоединения лежит при более длинных волнах, чем максимум поглощения самого дибенз-антрона; красители ряда дибензантрона синего цвета, а диметоксисоединения - синевато-зеленого. В то же время у диметоксисоединения наблюдается снижение интенсивности максимума поглощения. Старые представления о том, что субстантивные красители имеют длинные нитевидные молекулы приблизительно прямолинейной формы, основанные на исследованиях азокрасителей бензидино-вого ряда, должны быть пересмотрены, исходя из строения субстантивных лейкосоединений антрахиноновых кубовых красителей. Сродство сложного полициклического красителя с несколькими хи-нонными группировками в молекуле, например Индантренового хаки GG, по-видимому, объясняется связыванием молекулы красителя в подходящих точках с различными параллельно расположенными остатками целлюлозы, так что молекулы красителя играют роль мостиков или решетки в трехмерной системе связей. [8]
В ряду галоидзамещенных фенилуксусных кислот наблюдается следующая общая зависимость активности от строения. Углеводородные радикалы снижают активность соединения, тогда как одна метоксильная группа незначительно влияет на активность 2 3 6-тризамещенной фенил-уксусной кислоты, однако положение метоксильной группы имеет существенное значение. [9]
Структура декстрана I рассмотрена выше ( стр. Дек-стран II имеет строение, аналогичное строению декстрана I. Декстран III имеет разветвленную форму молекул, но, поскольку положение метоксильных групп в диметилглюкозе не установлено, остается не выясненным и положение боковых цепей. По данным, полученным при измерении осмотического давления, молекула декстрана состоит не менее чем из 200 глюкозных остатков. [10]
Высокой физиологической активностью для растений обладают замещенные фенилуксусные кислоты. В ряду галогензамещенных фенилуксусных кислот наблюдается следующая общая зависимость активности от строения. Среди моногалогензамещенных фенил-уксусных кислот наибольшую активность проявляют 2-галоген - и наименьшую - 4-галогенпроизводные. Из изученных хлорпроиз-водных фенилуксусной кислоты наибольшей гербицидной активностью обладает 2 3 6-трихлорфенилуксусная кислота. Введение в молекулу фенилуксусной кислоты углеводородных радикалов снижает активность соединения. Наличие одной метоксильной группы незначительно влияет на активность 2 3 6-тризамещенной фенил-уксусной кислоты, однако положение метоксильной группы имеет существенное значение. [11]
Для установления строения гликозидов, содержащих один моносахаридный остаток, необходимо установить природу моносахарида, строение агликона, размер окисного цикла моносахаридного остатка и конфигурацию гликозидной связи. Для решения первой задачи проводят гидролиз гликозида, после чего идентифицируют образовавшийся моносахарид ( см. гл. Для полифункциональных агликонов задача осложняется тем, что при этом возникает необходимость выяснения места присоединения углеводного остатка к агликону. Кроме того, некоторые природные агликоны ( например, агликоны сердечных гликозидов) лабильны в кислой среде, что затрудняет получение неизмененного агликона при гидролизе. В таких случаях прибегают к ферментативному гидролизу ( см. стр. Многие природные гликозиды содержат несколько моносахаридных остатков, соединенных друг с другом О-гликозидными связями. Установление строения таких соединений включает помимо решения перечисленных задач установление строения олигосахаридной цепи ( или цепей) методами, применяемыми в химии олигосахаридов ( см. гл. Для определения размера окисного цикла моносахаридного остатка применяют два метода: метилирование и перио-датное окисление. Первый метод заключается в получении метиловых эфиров гликозидов и их последующем гидролизе; метилированию подвергаются все спиртовые гидроксилы моносахаридного остатка, за исключением того, который принимал участие в образовании окисного цикла исходного гликозида. Поэтому установление положения метоксильных групп в полученном при гидролизе метилированном моносахариде позволяет установить, который из спиртовых гидроксилов участвовал в образовании цикла. [12]
Страницы: 1