Октаэдрическое положение
Cтраница 3
Резко выраженный релаксационный характер диэлектрической поляризации отсутствует. Это объясняется наличием ближнего порядка в распределении ионов В и В в октаэдрических положениях решетки при отсутствии дальнего порядка. [31]
Показатели преломления РЗГГ ( табл. 25.13) сравнительно слабо различаются между собой, несмотря на большое разнообразие в составах. На показатель преломления п гранатов слабо влияет замещение как в додэкаэдри-ческих, так и в октаэдрических положениях. Основной причиной различия п является различие в сорте ионов, занимающих тетраэдри-ческие позиции. На примере ГГГ и ГСГГ ( табл 25.13) видно, что введение ионов Nd3 и Сг3 вызывает лишь весьма небольшое ( на уровне 5 - 10 - 3) увеличение п этих кристаллов. [32]
Многочисленными опытами и расчетами установлено, что ионы с большим радиусом и низкой валентностью ( Mn2, Cd2, Zn2), как и небольшие ионы с высокой валентностью, стремятся в тетраэдрическое положение. Небольшие же ионы с низкой валентностью и большие ионы с высокой валентностью ( Ti4, Sn4) находятся в октаэдрическом положении. [33]
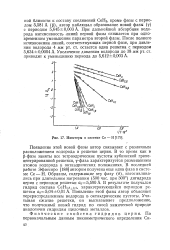 |
Изостеры в системе Се - Н. [34] |
Появление этой новой фазы автор связывает с различным расположением водорода в решетке церия. В то время как в р-фазе заняты все тетраэдрические пустоты кубической гране-центрированной решетки, у-фаза характеризуется размещением атомов водорода в октаэдрических положениях. Образцы, содержащие эту фазу ( 6), изготавливались при длительном нагревании ( 500 час. [35]
Энергия P ( v), которая определяется формулой (2.16) и количественно рассчитывается по формуле (2.24), характеризует лишь относительную тенденцию ионов к занятию октаэдрических положений; ее недостаточно для того, чтобы во всех случаях определить истинное распределение ионов. Конечно, эти возражения не существенны, если разность энергий Р ( v) соответствующих ионов велика. Тогда, очевидно, и разность энергий кристалла для обоих предельных случаев - обращенной и нормальной шпинели-имеет большую величину, так что в рассматриваемой температурной области энтропийный член TS не оказывает влияния на катионное распределение. [36]
При сравнении ферритов со структурами типа граната и шпинели обнаруживаются существенные различия в магнитном взаимодействии. В ферритах со структурой типа шпинели каждый ион железа, находящийся в октаэдриче-ском положении, может заметно взаимодействовать с двенадцатью другими ионами железа, также находящимися в октаэдрических положениях. Яфет и Киттель [23] первыми предположили, что в этом случае может не иметь места простое параллельное и антипараллельное расположение магнитных моментов ионов. [37]
В ZnFe2O4 градиент электрического поля наблюдается для ионов Fe3 в октаэдрическом окружении. Градиент электрического поля ионов Fe, находящихся в FeNiAlO4 и FeNiCrO4 в тетраэдрическом окружении, возникает от распределения ( № 2) и ( А13 и Сг3) в октаэдрических положениях. Для FeAl2O4, имеющего только однородные тетраэдрические положения, квадрупольные расщепления не обнаружены. Квадрупольные взаимодействия не вызваны кооперативными возмущениями в кристалле, так как они проявляются в Mgo o8Fe0) 02Al2O4, где кооперативность отсутствует. [38]
В этом кристалле атом азота образует ковалентные связи с четырьмя соседними атомами алюминия. ScN, TIN, ZrN, VN, NbN, TiC, ZrC, VC, NbC, TaC имеют структуру NaCl и состоят из атомов металла в плотной кубической упаковке с атомами азота или углерода в октаэдрических положениях. Так как атомы первого периода периодической таблицы не могут образовывать больше четырех ковалентных связей, то представляется вероятным, что октаэдрическая координация шести атомов металла вокруг каждого легкого атома включает резонанс ковалентных связей между шестью положениями. Структура Fe примерно такая же. [39]
 |
Зависимость между электроотрицательностью металлов и типом связи в их гидридах. [40] |
Для гидридов металлов III группы характерно, что из трех атомов водорода, которые они максимально могут присоединять, первые два атома заполняют тетраэдрические пустоты и более прочно связаны, чем третий атом водорода, который находится в октаэдрическом положении, в большей мере отвечающем ионной связи. [41]
Стереохимия соединений галоидов между собой изучена еще меньше. Если применить вышеизложенные соображения к 1С13 и 1РБ, то следует ожидать, что первое из этих соединений будет плоским, так как атом иода имеет две пары свободных электронов, a IF6 должен образовать квадратную пирамиду, в которой одна пара свободных электронов занимает шестое октаэдрическое положение. Трихлорид иода представляет собой желтое твердоэ вещество; в газообразном состоянии это соединение почти полностью диссоциировано на IC1 и С12; структура молекулы 1С13 до сих пор не установлена. Триго-нальная бипирамидальная конфигурация, приписанная IF6 в результате исследования методом диффракцин электронов, повидимому, неправильна, так как найденные в этой структуре межатомные расстояния являются сомнительными. Стереохимия иода в оксисосдннениях будет изложена ниже. [42]
У минералов группы монтмориллонита широко развит изоморфизм, особенно в октаэдрах. Черкасский монтмориллонит является диоктаэдрическим минералом. Октаэдрические положения заняты в нем в основном катионами алюминия и железа. Кроме того, незначительная часть кремния в тетраэдрах замещена алюминием. [43]
В структурах, подобных диоктаэдрическому монтмориллониту ( см. рис. 141 и 142), алюминий может быть полностью замещен магнием. Для сохранения электронейтральности решетки три иона магния должны заменить два иона алюминия. Оставшаяся вакантной треть октаэдрических положений может быть заполнена, образуя триоктаэдрическую структуру. [44]
Такое замещение уже давно рассматривается как причина катион-ного обмена у глин, подобных монтмориллониту. Разумеется, два соседних иона А13 могут быть замещены тремя ионами Mg2; такое изменение представляет превращение, например, гидрар-гиллита в бруцит. Оно возможно потому, что ионы алюминия занимают только два из трех соседних октаэдрических положений. В этом случае положительный заряд нейтрализуется иолом магния, в результате чего структура оказывается каталитически не активной. [45]
Страницы: 1 2 3 4