Последняя закономерность
Cтраница 2
Молярное соотношение оснований выражает количественный состав азотистых компонентов в нуклеиновых кислотах. Важность последней закономерности особенно проявляется при формировании двойной спирали ДНК. [16]
И здесь наблюдаются те же закономерности: селективность уменьшается при переходе от второй триады к третьей. Селективность триад увеличивается слева направо. Последняя закономерность нарушается в случае иридия, который склонен катализировать образование парафина при гидрогенизации пропадиена. Факторами, обуславливающими селективность, могут быть а) относительная прочность адсорбции бутадиена-1, 3 и бутенов на каждом металле и б) активность каждого металла в гидрогенизации бу-тена. [17]
Бильтц также установил, что частная теплота образования аммиаката с увеличением числа присоединенных молекул аммиака уменьшается. Впрочем, последняя закономерность является лишь частным случаем рассмотренного выше правила Вертело [3] об истощении энергии системы по мере усложнения ее состава. [18]
Удельный вес вещества является одним из факторов, определяющих распределение, паров этого вещества в воздухе. Пары веществ с - удельным весом меньше удельного веса воздуха при одинаковых температурных условиях поднимаются в верхнюю зону, поэтому, проходя через относительно толстый слой воздуха ( при выделении паров в нижней зоне), они быстро перемешиваются с ним, загрязняя значительные пространства и создавая наиболее высокие концентрации В верхней зоне ( если оттуда нет механической или естественной вытяжки), При удельном весе веществ больше удельного веса воздуха выделяющиеся пары скапливаются преимущественно в нижней зоне, создавая там наиболее высокие концентрации. Однако следует заметить, что эта последняя закономерность часто нарушается, когда имеют место тепловыделения или сами пары выделяются в нагретом виде. В этих случаях, несмотря на большой удельный вес, конвекционными потоками нагретого воздуха пары увлекаются в верхню зону и также загрязняют воздух. Все эти закономерности необходимо учитывать при размещении рабочих мест на разных уровнях цеха и при оборудовании вытяжной вентиляции. [19]
Условия анализа и природа вещества влияют на 8 в основном так же, как и на число теоретических тарелок ( ср. Последняя закономерность противоположна зависимости числа теоретических тарелок от приведенного времени удерживания, отнесенного к мертвому времени, где для малых & г получались особенно большие числа теоретических тарелок. [20]
Изменения температуры в стволе скважины являются итогом тепловых процессов, происходящих как в пласте, так и в самом стволе скважины. Температура на забое скважины управляется тепловыми явлениями в пласте. Но по мере удаления от забоя постепенно теряется влияние забойной температуры, и на устье скважины температура потока обычно не имеет ощутимой связи с забойной температурой. Последняя закономерность сохраняет силу и для нисходящих потоков в стволе нагнетательной скважины, где температура нагнетаемого агента на забое при ограниченных расходах практически не зависит от температуры на поверхности. [21]
Эффективность разделения, выраженная остротой разделения 8, не зависит от А. Условия анализа и природа вещества влияют на 8 в основном так же, как и на число теоретических тарелок ( ср. Последняя закономерность противоположна зависимости числа теоретических тарелок от приведенного времени удерживания, отнесенного к мертвому времени, где для малых А. [22]
Таким образом, при решении задачи о структуре сложного атома приходится прибегать к приближенным методам. Один из простейших методов заключается в следующем. В основном, невозбужденном состоянии атома электроны находятся на наинизших возможных квантовых уровнях. При этом для получения результатов, отвечающих опыту, пришлось предположить, что в одном квантовом состоянии, определяющемся тройкой квантовых чисел n, I, mi, может находиться не более двух электронов. Последняя закономерность была указана Паули и носит название принципа ( или запрета) Паули. Энергия квантовых состояний по-прежнему в основном определяется главным квантовым числом п, но, в отличие от атома водорода, состояния с различными / обладают разной энергией из-за электрического взаимодействия между электронами. Минимальную энергию имеют состояния с малыми I. Состояния с большими I отвечают большей энергии. При Н 0 состояния с различными т / обладают одинаковой энергией. В табл. 1.1 приведено количество мест для электронов в различных квантовых состояниях. [23]
Сопоставление дефектов масс обнаруживает новые, еще не объясненные закономерности. Дефекты масс всех изотопов ( как стабильных, так и радиоактивных) данного элемента в функции массового числа А располагаются на двух квадратичных параболах, одна из которых охватывает изотопы с четными А, а другая - с нечетными. На рис. 5 представлен пример таких пар парабол, относящийся к изотопам селена. Далее было показано [148], что если соединить плавной кривой вершины таких парабол, относящихся к четным А и Z, то на них с точностью до 0 003 ед. Эта последняя закономерность охватывает всю таблицу элементов. [24]
Только применительно к Tpaiic-Pt ( PR3) 2CL ( транс-конфигурация которого установлена химическими методами) оказалось возможным получить ориентировочные данные, свидетельствующие о практическом отсутствии у этого соединения диполыюго момента. ОсновЕлваясь на этом, Иенсеп пришел к заключению, что определенные методами Верпера и Гринберга конфигурации изомерных аммиакатов и аминатов двухвалентной платины соответствуют действительности, но что установленные при изучении аммиакатов и аминатов закономерности образования платосолей ( цис-закономерность Нейроне и транс-закономерность Иергенсена) не применимы для случаев, когда аддендами являются тиоэфиры и третичные фосфипы. Для объяснения этого различного отношения Иенсен выдвинул предположение, что закономерности Пейроне и Иергенсепа выполняются, если речь идет об аммиаке, первичных аминах или вообще о первично замещенных аддеидах, в то время как третично замещенные адденды должны показывать уклонения от этих закономерностей. Такое объяснение казалось нам недостаточно глубоким. Мы знаем, что и закономерность Пейроне и закономерность Иергенсена являются следствием закономерности транс-влияния, и нам известно, что под влиянием этой последней закономерности могут иметь место отступления от закономерности Пейроне. Уже в 1940 г. при составлении монографии Введение в химию комплексных соединений один из пас глубже проанализировал следствия, вытекающие из теории транс-влияния, и пришел к выводу, что закономерности образования и реагирования платосолей, установленные на примере аммиакатов и аминатов, не имеют абсолютного характера, но что применимость или неприменимость их к каждому частному случаю зависит от соотношения величин транс-влияния групп, находящихся в исходном комплексе, и групп, вновь вступающих в комплекс. Уели транс-влияние групп, вновь вступающих в комплекс типа Pta4, где х - какая-либо координированная при ионе двухвалентной платины кислотная или нейтральная группа, меньше, чем транс-влияние х, то должны получаться соединения цнс-конфигурации. Уели же транс-влияние вновь вступающих групп больше, чем транс-влияние х, то первично должны возникать соединения транс-конфигурации. Подчеркиваем, что при этом безразлично, будет ли х кислотным остатком или нейтральной молекулой. [25]
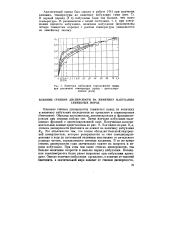 |
Кинетика набухания тереклинской глины при различной температуре ( среда - дистиллированная [ вода. [26] |
Как видно из рис. 8, а, степень дисперсности бентонита не влияет на величину набухания / fjj. Это объясняется тем, что глины обладают большой внутренней поверхностью, которая раскрывается ла счет само диспергирования в воде до постоянной величины независимо от начального размера частиц, определяемого ситовым анализом. В то же время степень дисперсности глин значительно влияет на скорость и период набухания. Последняя закономерность более резко выражена при набухании аргиллита. [27]
В этой книге, впоследствии переведенной на русский язык, приведена таблица элементов, в которой 44 элемента ( из 63 известных в то время), были расставлены в 6 столбцах в соответствии с их валентностью ( высшей) по водороду. Как видно из этой таблицы и приложенной к ней второй небольшой таблицы, автор фиксирует внимание на разностях атомных весов между сходными элементами, расставленными в вертикальных группах: 1-я группа - углерода, 2-я - азота, 3-я-кислорода, 4-я - галогенов, 5-я - щелочных металлов и 6-я - щелочноземельных металлов. В основной таблице, объединяющей эти группы, 28 элементов расставлены в порядке возрастания их атомных весов, что, как мы уже видели, в то время не было новостью. Вторая таблица может рассматриваться как извлечение из первой. Однако, если в первой таблице фигурируют тетрады и пентады, подобранные достаточно хорошо, во вторую таблицу входят элементы, не укладывающиеся в группы первой таблицы. Разности атомных весов между соответствующими элементами пентад приблизительно постоянны. Эта последняя закономерность была отмечена еще ранее. [28]
Страницы: 1 2