Основная закономерность - сорбция
Cтраница 1
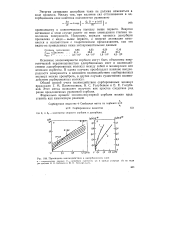 |
Проявление взаимодействия в адсорбционном слое. [1] |
Основные закономерности сорбции могут быть объяснены энергетической неравноценностью адсорбционных мест и взаимодействием адсорбированных молекул между собой и молекулами или атомами сорбента. В одних случаях преобладает влияние неоднородности поверхности и влиянием взаимодействия сорбированных молекул можно пренебречь, в других случаях существенно взаимодействие сорбированных молекул. [2]
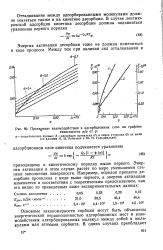 |
Проявление взаимодействия в адсорбционном слое на графике зависимости р / а от р. [3] |
Основные закономерности сорбции могут быть объяснены энергетической неравноценностью адсорбционных мест и взаимодействием адсорбцированных молекул между собой и молекулами или атомами сорбента. [4]
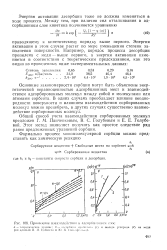 |
Проявление взаимодействия в адсорбционном слое. [5] |
Основные закономерности сорбции могут быть объяснены энергетической неравноценностью адсорбционных мест и взаимодействием адсорбированных молекул между собой и молекулами или атомами сорбента. В одних случаях преобладает влияние неоднородности поверхности и влиянием взаимодействия сорбированных молекул можно пренебречь, в других случаях существенно взаимодействие сорбированных молекул. [6]
Основные закономерности сорбции из растворов сохраняются и при извлечении урана из пульп, содержащих до 40 - 50 % твердого вещества. [7]
Рассмотрим основные закономерности сорбции электролитов в гидрофобные и гидрофильные полимеры. [8]
Рассмотрены основные закономерности сорбции биологически активных веществ ионитами, связанные со своеобразием их структуры и невысокой устойчивостью. Разработаны особые принципы выбора ионитов, предназначенные для выделении II и шпни органических - Ш ттн. [9]
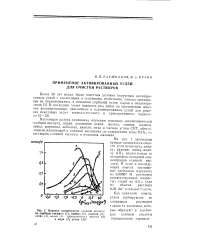 |
Влияние концентрации соляной кислоты на сорбцию висмута ( 1, свинца ( 2, кадмия ( 3, цинка ( 4, индия ( 5. трехвалентного железа ( 6 и меди ( 7 углем СКТ. [10] |
Настоящая работа посвящена изучению основных закономерностей сорбции висмута, индия, алюминия, церия, железа, свинца, кадмия, цинка, марганца, кобальта, никеля, меди и магния углем СКТ, обезволенным, плавиковой и соляной кислотами до содержания золы 0 3 %, из растворов соляной кислоты и роданида аммония. [11]
Прежде всего разделение в хроматографических колонках происходит за счет различной сорбируемости компонентов смеси, а в конечном итоге за счет различий межмолекулярных взаимодействий. Поэтому следует рассмотреть основные закономерности сорбции ( адсорбции и растворения), а также основные типы межмолекулярных взаимодействий. [12]
Применение ионного обмена и других сорб-ционных методов непосредственно к пульпам позволило радикально усовершенствовать технологию переработки многих руд. Установлено, что основные закономерности сорбции урана ионитами из растворов сохраняются при сорбции из пульп, содержащих до 40 - 50 % твердого. Наблюдаемые иногда различия в кинетических характеристиках нонитов объясняются влиянием кинетики десорбции ионов металла из твердой фазы пульпы. [13]
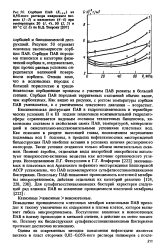 |
Сорбция ПАВ С8Гц0 из 0 5 % - ного раствора кварцевым песком ( 1 - 3 и кальцитом ( 4 - 6 при температурах 20 ( JP, 4, 50 ( 2, 5 и 80 С С., 6 по Н.Д. Таирову. [14] |
Рисунок 50 отражает основные закономерности сорбции ПАВ. Сорбция ПАВ породами относится к категории физической сорбции и, следовательно, при прочих равных условиях определяется величиной поверхности сорбента. [15]
Страницы: 1 2