Понижение - концентрация - серная кислота
Cтраница 2
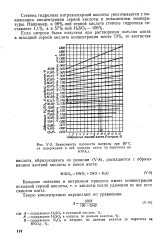 |
Зависимость плотности нитрозы при 20 С. [16] |
Степень гидролиза нитрозилсерной кислоты увеличивается с понижением концентрации серной кислоты и повышением температуры. [17]
Степень гидролиза нитрозилсерной кислоты увеличивается с повышением температуры и понижением концентрации серной кислоты. [18]
Экспериментально установлено, что скорости реакции сульфирования возрастают с повышением концентрации серной кислоты, и наоборот - при понижении концентрации серной кислоты уменьшается скорость сульфирования. [19]
Это объясняется рядом обстоятельств. С понижением концентрации серной кислоты увеличивается степень ее электролитической диссоциации, что повышает число и концентрацию свободных ионов - носителей электрических зарядов. Однако при очень сильном разбавлении кислоты, хотя электролитическая диссоциация приближается к максимуму, объемная концентрация ионов значительно падает. При большой степени электролитической диссоциации, но недостаточном разбавлении кислоты, близость друг к другу разноименных ионов замедляет их движение во взаимопротивоположных направлениях. [20]
 |
Влияние концентрации H2SO4. [21] |
Из данных табл. 9 видно, что при содержании кислоты в осадительнои ванне 18 - 20 г / л волокно имеет необходимую высокую прочность в петле. С понижением концентрации серной кислоты в ванне уменьшается содержание кислоты в жгуте и несколько понижается скорость разложения ксантогената целлюлозы. Указанные факторы, по-видимому, обусловливают возможность частичного набухания волокна в процессе вытягивания за счет - выделяющегося при разложении ксантогената целлюлозы едкого натра. Полученное в этих условиях полинозное волокно имеет прочность в петле 7 - 8 гс / текс, что соответствует лучшим образцам зарубежных полинозных волокон. [22]
С понижением концентрации серной кислоты светопоглощение ниобия понижается и смещается в ультрафиолетовую область, а поглощение комплекса титана в видимой области увеличивается. [23]
При понижении концентрации серной кислоты разбавлением ее водой или при смешивании кислот различной концентрации выделяется тепло. На рис. 7 показано количество тепла, выделяющегося при разбавлении 100 % - ной серной кислоты при 15 С до 50 % - ной. [24]
Состав пара над серной зовавшиеся над растворами кислотой при температуре кипения, серной кислоты различной концентрации при температуре кипения. Из рисунка видно, что с понижением концентрации серной кислоты содержание H2SO4 в парах очень сильно уменьшается. [25]
Процесс ведут при очень интенсивном барботировании. Концентрация свободной кислоты в растворе должна быть не выше 0 5 %, так как при более высокой концентрации происходит интенсивное растворение железа. Понижение концентрации серной кислоты достигается либо разбавлением раствора, либо добавкой известкового молока. Медный шлам, содержащий 60 - 80 % Си, периодически выгружают и отправляют на переплавку. Расход железа составляет примерно 3 кг на 1 кг меди. Процесс рентабелен в больших производствах. [26]
В химической и нефтеперерабатывающей промышленности широко применяется серная кислота. Характер коррозии металлов в присутствии концентрированной и разбавленной кислот совершенно различен. Концентрированная кислота ( концентрация более 80 %) не вызывает существенного разрушения даже углеродистых сталей. С понижением концентрации серной кислоты ее агрессивность возрастает. Например, в 5 % - ной серной кислоте стойкость проявляют только кремнистый чугун, некоторые марки хромонике-левых сталей ( типа ОХ23Н28МЗДЗТ), алюминий, медь, свинец. Это объясняется тем, что в присутствии концентрированной кислоты, являющейся сильным окислителем, на поверхности углеродистой стали и чугуна образуются пленки окислов, предохраняющие металл от дальнейшего коррозионного разрушения. [27]
Сульфирование, как и хлорирование, асфальтепов изучается сравнительно давно. Им определены оптимальные условия процесса ( расход 20 % - ного олеума - 4 г / г сырья, 100 С, продолжительность сульфирования 2 ч) с це /: ыо получения ионообменных материалов. Реакции сульфирования сопровождаются процессами деструктивного окисления боковых алкильных цепей и алицикли-ческих фрагментов с образованием карбоксильных и фенольных групп. С понижением концентрации серной кислоты протекает преимущественно реакция окисления. В растворе четыреххлори-стого углерода происходит также дегидрирование алиниклических колец до ароматических и окислительная конденсация сульфопро-дуктов. [28]
Образование кристаллов ангидрита связано с дегидратацией первоначально выделяющегося полугидрата. В растворе, содержащем 50 % Р2О5, при 90 перекристаллизация начинается только через 6ч и заканчивается после 30ч ( стр. Дегидратация полугидрата ускоряется с увеличением концентрации P2Os, а также при наличии в растворе серной кислоты. Так, в кислоте, содержащей в растворе 47 - 50 % Р2О5 и больше 5 % H2SO4, дегидратация при 100 заканчивается в течение 20 - 40 мин. Образующиеся кристаллы ангидрита имеют прямоугольную форму и длину 15 - 30 мк, а ширину - 6 - 10 мк. С понижением концентрации серной кислоты до 3 % продолжительность полного превращения полугидрата при 100 увеличивается до 80 - 85 мин. При этом получаются значительно более крупные кристаллы, имеющие также прямоугольную форму, с размерами, например, 30 - 40 X 6 - 8 мк. [29]
Страницы: 1 2