Понижение - температура - процесс
Cтраница 1
 |
Влияние концентрации с раствора ( цифры на кривых на скорость деструкции ДЭА при Р4 1 МПа и / 205 С.| Влияние температуры на скорость деструкции ДЭА ( среда СО2 - водный раствор ДЭА. [1] |
Понижение температуры процесса позволяет увеличить производительность абсорберов и уменьшает эксплуатационные расходы на дальнейшую обработку газа. Однако это несколько увеличивает растворимость углеводородов в растворе, что снижает его избирательность. Кроме того, повышается вероятность гидратообразования в системе. [2]
 |
Технологическая схема получения A1F3 в непрерывном режиме. / - шнековый питатель. 2 - бак постоянного уровня. 3 - электрообогрев. 4 - подогреватель. 5 - реактор. [3] |
Понижение температуры процесса приводит к увеличению продолжительности реакции, потерям алюминия вследствие неполного взаимодействия, замедлению фильтрации за счет образования диоксида кремния с развитой удельной поверхностью. [4]
Понижение температуры процесса, таким образом, сдвигает границу периодов в область более высоких температур размягчения. Изменение расхода воздуха влияет на положение этой границы лишь при низкой температуре. [5]
Понижение температуры процесса приводит к уменьшению эффективного размера пор. [6]
Понижение температуры процесса до 850 - 800 С ведет к стабилизации состава получаемого газа, однако при 850 С также наблюдается пиролиз метана, как пишут авторы, во второй половине опыта. При наличии в исходной смеси водяного пара разложение метана на С и На не происходит. [7]
 |
Влияние концентрации с раствора ( цифры на кривых на скорость деструкции ДЭА при Р. 4 1 МПа и 205 С.| Влияние температуры на скорость деструкции ДЭА ( среда С02 - водный раствор ДЭА. [8] |
Понижение температуры процесса позволяет увеличить производительность абсорберов и уменьшает эксплуатационные расходы на дальнейшую обработку газа. Однако это несколько увеличивает растворимость углеводородов в растворе, что снижает его избирательность. Кроме того, повышается вероятность гидратообразования в системе. [9]
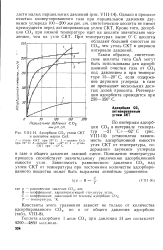 |
Адсорбция СО2 углем СКТ и цеолитом марки СаА. [10] |
Понижение температуры процесса способствует значительному увеличению адсорбционной емкости угля. [11]
Понижение температуры процессов очистки возможно переводом очищаемого вещества в форму какого-либо летучего или легкоплавкого соединения. [12]
Понижение температуры процесса абсорбции способствует снижению расхода абсорбента. Увеличение расхода абсорбента приводит к росту энергетических затрат при нагреве перед десорбером и охлаждении перед абсорбером. [13]
Понижение температуры процесса абсорбции позволяет снизить удельный расход абсорбента и уменьшить необходимое число тарелок. В промышленных условиях температура абсорбции зависит главным образом от применяемого охлаждающего агента. В современных абсорбционных установках, обеспечивающих извлечение практически всех компонентов газа, включая этан, экономически оправдано ведение процесса при пониженных температурах с использованием специальных хладагентов: испаряющихся аммиака, пропана и др. В этом случае затраты на сооружение и эксплуатацию специальных холодильных установок быстро окупаются за счет сокращения капитальных и эксплуатационных затрат на другое оборудование. [14]
Понижение температуры процесса полимеризации ( способствующее получению каучуков лучшего качества) приводит к снижению скорости реакции, так как уменьшается скорость образования свободных радикалов. Суть инициирования полимеризации такими системами заключается в интенсивном образовании радикалов при взаимодействии между окислителем и восстановителем. Например, при введении в полимеризационную систему солей двухвалентного железа скорость распада перекиси бензоила увеличивается в сотни раз. Часто такой быстрый распад инициатора не требуется, так как инициатор может израсходоваться задолго до полной конверсии мономера. Для уменьшения скорости окислительно-восстановительных процессов соли железа вводят ( В систему в виде труднорастворимых комплексов ( например, пирофосфатных); это обеспечивает низкую концентрацию ионов Р в системе, и скорость распада перекиси уменьшается. [15]
Страницы: 1 2 3 4