Понижение - давление - насыщенный пар
Cтраница 4
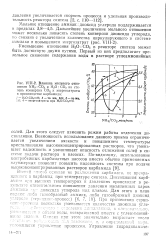 |
Влияние мольного отношения NH3. СО2 и Н2О. СО2 на степень конверсии СО2 и энергозатраты в производстве карбамида.. - Н2О. СО20. 2 - то же, 0 5. 3 - то же, 1 0. 4 - энергозатраты при Н2О. СО20. [46] |
ВТОРОЙ - пособ основан на разложении карбамата, ке превращенного в карбамид при температуре синтеза. Диссоциация карбон высоких температурах и давлениях происходит в ре-относительного понижения давления насыщенных паров г v диоксида углерода над плавом. [47]
Возрастание числа частиц растворенного вещества вследствие электролитической диссоциации вызывает не только увеличение осмотического давления. Понижение температуры замерзания раствора, повышение его температуры кипения и понижение давления насыщенного пара тоже пропорциональны действительному числу частиц. Тот же множитель t входит и в соответствующие выражения для повышения температур кипения раствора и понижения давления его пара. Следовательно, определение любого из этих свойств также дает возможность вычислить степень диссоциации электролита. [48]
Возрастание числа частиц растворенного вещества вследствие электролитической диссоциации вызывает не только увеличение осмотического давления. Понижение температуры замерзания растворителя, повышение его температуры кипения и понижение давления насыщенного пара тоже пропорциональны действительному числу частиц. Поэтому, например, понижение температуры замерзания растворителя в растворах электролитов выражается не формулой & ся Еяс, относящейся к обычным растворам ( стр. E c, где / - изотонический коэффициент, связанный со степенью электролитической диссоциации а. Тот же множитель / входит и в соответствующие выражения для повышения температур кипения растворителя и понижения давления его пара. Следовательно, определение любого из этих свойств также дает возможность вычислить степень диссоциации электролита. [49]
Такой характер зависимости может быть связан с переходом в этой области температур от гетерогенной системы С J к гомогенной. При этом происходит усиление взаимодействия компонентов с образованием фрагментов жидкокристаллической упорядоченности, что и проявляется в некотором понижении давления насыщенного пара с ростом температуры. [50]
Итак, весь приведенный выше материал показывает, что между понижением температуры плавления ( при повышении температуры кипения) раствора и концентрацией труднолетучего компонента имеется простая линейная зависимость, которая получила название криоскопического и эбуллиоскопического законов Рауля. В качестве следствия отмечалось, что при равной температуре давление пара над таким раствором должно быть меньше давления пара над чистым растворителем. Это изотермическое понижение давления насыщенного пара над раствором может быть учтено количественно. [51]
Рассмотрим процесс конденсации паров в охлаждаемой снаружи трубе при постоянной температуре поверхности конденсации Т2 по всей длине трубы. После образования капель начинается коагуляция, в процессе которой число капель уменьшается, а размер их увеличивается. Это приводит к понижению давления насыщенного пара над каплями и, следовательно, к конденсации паров на поверхности капель. Вследствие выделения тепла конденсации температура капель становится выше температуры окружающей парогазовой смеси и происходит теплоотдача от капель к газу. [52]
Известно, что ряд свойств разбавленных растворов не зависит от природы растворенного вещества, а только от его концентрации. Такие свойства называются коллигативными. К ним относятся осмотическое давление, понижение давления насыщенного пара над раствором, понижение температуры кристаллизации и повышение температуры кипения раствора. [53]
Страницы: 1 2 3 4