Молекулярное понижение - температура - замерзание
Cтраница 1
 |
Криоскопические постоянные некоторых растворителей. [1] |
Молекулярное понижение температуры замерзания Е, для обычных растворителей известно. [2]
Молекулярное понижение температуры замерзания растворителя Е3 зависит только от его химической природы и не зависит от концентрации раствора и химического состава растворенного вещества. [3]
Молекулярное понижение температуры замерзания водных растворов окиси этилена6 равно dt / N 1 7, где N - число молей окиси этилена, растворенных в 1000 г воды. [4]
Постоянная К называется молекулярным понижением температуры замерзания или криоскопической постоянной; величина ее зависит от природы растворителя. Если растворенное вещество способно подвергаться диссоциации, а растворитель - ассоциации, наблюдается отклонение понижения температуры замерзания при изменении концентрации растворов от прямолинейности. [5]
Криоскопическая константа К ( молекулярное понижение температуры замерзания) растворителя представляет собой понижение температуры замерзания, вызываемое растворением 1 моль неднссоцнирующсго вещества в 1000 г растворителя, при условии образования идеального раствора. [6]
С - криоскопическая постоянная или молекулярное понижение температуры замерзания растворителя. Повышение температуры кипения и понижение температуры замерзания не зависит от природы растворенного неэлектролита, а зависит только от его моляль-ной концентрации. Растворы различных веществ равной концентрации изменяют на одну и ту же величину температуру кипения и температуру замерзания данного растворителя. Константы Е и К представляют собой повышение температуры кипения раствора или понижение температуры замерзания его при растворении 1 г-моля неэлектролита в 1000 г растворителя. [7]
Коэффициент пропорциональности К в уравнении (18.7) называется криоскоп и ческой константой, или молекулярным понижением температуры замерзания. Численное значение криоскопической константы различно для различных растворителей, но для данного растворителя представляет постоянную величину, независимую от природы растворенного вещества. [8]
Согласно с этим указанное превращение сопровождается по Рекура [75] выделением теплоты, а по исследованиям А. В. Сперанского [76] и Маркетти [77] - увеличением молекулярной электропроводности и молекулярного понижения температуры замерзания растворов. [9]
Условные обозначения: М - молекулярный вес; А - концентрация в граммах безводного вещества на 100 г воды; га - концентрация в молях безводного вещества на 1000 г воды; Д / - понижение температуры замерзания, С; ( ДОд - молекулярное понижение температуры замерзания, С. [10]
При криоскопическом исследовании концентрированных растворов получаются результаты, противоречившие теории электролитической диссоциации, согласно которой с увеличением концентрации степень диссоциации должна уменьшаться. Следовательно, и молекулярное понижение температуры замерзания должно с увеличением концентрации раствора все время непрерывно уменьшаться. [11]
Эта величина называется молекулярным понижением температуры замерзания, или крио скопияеской константой растворителя. [12]
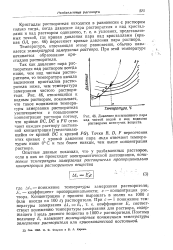 |
Давление насыщенного пара. [13] |
Концентрацию с принято выражать в молях на 1000 г ( или иногда на 100 г) растворителя. Поэтому величину Е3 называют молекулярным понижением температуры замерзания растворителя или криоскопической постоянной. [14]
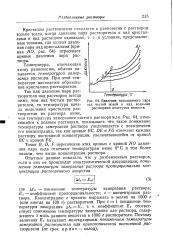 |
Давление насыщенного пара. [15] |
Страницы: 1 2