Понятие - скорость
Cтраница 2
Понятие скорости силовой линии полезно также для интуитивной оценки потока электромагнитной энергии в плазме. [16]
Понятие скорости распространения турбулентного пламени относится к явлению горения в топливной смеси, имеющей турбулентные пульсации различного масштаба, которые существенно увеличивают действительную поверхность горения. [17]
Поясним понятие скорости распространения изотермы. [18]
Распространим теперь понятие скорости на случай любого криволинейного и неравномерного движения. [19]
Используют также понятие эмпирической скорости k3, соответствующее точке перегиба, очевидно, она представляет собой максимальную скорость, наблюдаемую в ходе процесса. [20]
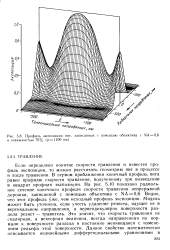 |
Профиль экспозиции пит, записанных с помощью объектива с NA 0 6 и скважностью 70 % ( р1100 нм. [21] |
Если определено понятие скорости травления и известен профиль экспозиции, то можно рассчитать геометрию пит в процессе и после травления. В первом приближении конечный профиль пита равен профилю скорости травления, полученному при возведении в квадрат профиля экспозиции. Видно, что этот профиль уже, чем исходный профиль экспозиции. Модель может быть уточнена, если учесть удаление резиста, идущее не в вертикальном направлении, а перпендикулярно поверхности раздела резист - травитель. Это значит, что скорость травления не скалярная, а векторная величина, всегда направленная по нормали к поверхности раздела и постоянно меняющаяся с изменением рельефа этой поверхности. [22]
Определим теперь понятие скорости поверхностной рекомбинации s, представляющей собой скорость электронно-дырочной рекомбинации на поверхности материала. [23]
Установим теперь понятие скорости неравномерного процесса изменения. [24]
При анализе понятия скорости предполагалось, что утверждение о нахождении материальной точки в двух сколь угодно близких точках пространства в два сколь угодно близкие момента времени имеет объективный смысл. [25]
Для формирования понятий скорости и ускорения был необходим метод исчисления бесконечно малых, связанный с именами Ньютона и Лейбница. Современные представления требуют для этих понятий еще более сложного математического описания. [26]
Физический смысл понятия скорости витания следующий. При свободном падении твердого тела в среде неподвижного воздуха оно движется ускоренно до тех пор, пока сила сопротивления воздушной среды не сравняется с весом тела; после этого падение тела продолжается при постоянной скорости. Если поток воздуха движется вверх со скоростю, равной постоянной скорости свободного падения, тело будет находиться в колебательном состоянии на одном уровне. Эту постоянную скорость свободного падения твердого тела принято называть скоростью витания. [27]
Универсального определения понятия скорости гетерофазного химического процесса не существует. Для гомогенных гетерофазных процессов обычно пользуются определением ( II. У объем той фазы, в которой проходит химическое превращение. Например, при разложении перекиси водорода в растворе под скоростью реакции по перекиси водорода понимают изменение концентрации перекиси водорода в единицу времени, а под скоростью реакции по кислороду - изменение количества кислорода в газовой фазе ( предполагается, что количеством растворенного кислорода можно пренебречь), отнесенное к единице объема раствора. Использовать в качестве меры скорости реакции изменение концентрации кислорода в газовой фазе нельзя, поскольку объем газовой фазы может изменяться вне всякой связи с разложением перекиси водорода. Можно, например, проводить реакцию в системе, в которой давление поддерживается постоянным. При этом производная от концентрации кислорода в газовой фазе будет равна нулю, с какой бы скоростью ни проходила реакция в растворе. [28]
Универсального определения понятия скорости гетерофазного химического процесса не существует. Для гомогенных гетерофаз-ных процессов обычно пользуются определением (II.7), понимая под V объем той фазы, в которой проходит химическое превращение. Например, при разложении перекиси водорода в растворе под скоростью реакции по перекиси водорода понимают изменение концентрации перекиси водорода в единицу времени, а под скоростью реакции по кислороду - изменение количества кислорода в газовой фазе ( предполагается, что количеством растворенного кислорода можно пренебречь), отнесенное к единице объема раствора. Использовать в качестве меры скорости реакции изменение концентрации кислорода в газовой фазе нельзя, поскольку объем газовой фазы может изменяться вне всякой связи с разложением перекиси водорода. Можно, например, проводить реакцию в системе, в которой давление поддерживается постоянным. При этом производная от концентрации кислорода в газовой фазе будет равна нулю, с какой бы скоростью ни проходила реакция в растворе. В равной степени нельзя использовать в качестве меры скорости этой реакции изменение концентрации кислорода в растворе, поскольку она изменяется не только в результате образования его из перекиси водорода, но и в результате выделения его в газовую фазу. [29]
Нетрудно распространить это понятие скорости при прямолинейном и равномерном движении на любое криволинейное и неравномерное движение точки. [30]
Страницы: 1 2 3 4