Тепловая поправка
Cтраница 3
С-С и С - Н - и последующего образования СОа и Н О; АЛ - f - В - число перемещающихся электронов для нормальных парафинов ( А и В - число атомов углерода и водорода в молекуле); р - число смещенных электронов в молекуле вещества ( смещенными считаются электроны атомов водорода и углерода, связанные с кислородом); k - число одинаковых заместителей в молекуле и А - соответствующая данному заместителю тепловая поправка, учитывающая изменение электронной структуры у нормальных парафинов вследствие поляризации связей, вызываемой введением заместителя. [31]
Аддитивные атомно-структурные методы расчета основаны на допущении, что энтальпия образования органических соединений в стандартном состоянии является аддитивной функцией вкладов различных групп атомов, составляющих молекулу. В этих методах используются табличные данные, содержащие тепловые поправки для различных замещающих групп. [32]
Более точные результаты дает метод тепловых поправок, так как в нем приближенно учитывается влияние соседних атомов на энергию связей в органических соединениях. В этом методе используется ряд таблиц, содержащих тепловые поправки для разного рода замещающих групп. [33]
Интенсивности измерены сцинтилляционным счетчиком. Для уточнения использован метод наименьших квадратов с введением анизотропных тепловых поправок для 4400 отражений. [34]
Этот метод не является в достаточной мере точным, так как тепловая поправка азогруппы ( по вычислениям автора) меняется для различных соединений в довольно широких пределах и, невидимому, не является столь постоянной, как тепловые поправки других заместителей. [35]
Если в таблицах стандартных термодинамических величин отсутствуют данные по теплотам образования или теплотам сгорания, то эти величины можно вычислить при помощи различных приближенных методов. Наиболее употребительными методами расчета теплот образования являются методы расчета по энергиям связи, при помощи тепловых поправок и метод сравнительного расчета. [36]
Теплота реакции нитрозирования в большинстве случаев не может быть вычислена с помощью метода Караша, так как тепловая поправка на нитрозогруппу ( NO) колеблется в весьма широких пределах в зависимости от наличия в ядре ароматического углеводорода прочих заместителей. Кроме того, в ряде случаев бывает затруднительным установить, какое именно строение имеют в момент образования продукты нитрозирования, так как им, как известно, приписываются формы и нитрозосоединений и оксимов. [37]
Этот метод не является в достаточной мере точным, так как тепловая поправка азогруппы ( по вычислениям автора) меняется для различных соединений в довольно широких пределах и, невидимому, не является столь постоянной, как тепловые поправки других заместителей. [38]
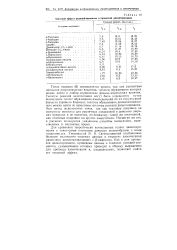 |
Тепловой эффект реакций-элементов в процессах диазотиропания. [39] |
Тепло реакции ( б) определяется просто, так как реагентами являются неорганические веихества, теплоты образования которых можно найти в любом справочнике физико-химических величин. Теплоты реакций азосочетания могут быть определены путем вычисления тешют образования азосоединений по их структурной формуле ( правило Караша), теплоты образования диазосоставляю-щих можно найти по известным теплотам реакций диазотирования. Этот метод недостаточно точен, так как тепловая поправка на азогруппу меняется для различных соединений в довольно широких пределах и не является, по-видимому, такой же постоянной, как тепловые поправки на другие заместители. Несмотря на это, в расчетах пользуются указанным способом вычисления, единственным в настоящее время. [40]
 |
Тепловой эффект реакций-элементов в процессах диазотиропания. [41] |
Тепло реакции ( б) определяется просто, так как реагентами являются неорганические веихества, теплоты образования которых можно найти в любом справочнике физико-химических величин. Теплоты реакций азосочетания могут быть определены путем вычисления тешют образования азосоединений по их структурной формуле ( правило Караша), теплоты образования диазосоставляю-щих можно найти по известным теплотам реакций диазотирования. Этот метод недостаточно точен, так как тепловая поправка на азогруппу меняется для различных соединений в довольно широких пределах и не является, по-видимому, такой же постоянной, как тепловые поправки на другие заместители. Несмотря на это, в расчетах пользуются указанным способом вычисления, единственным в настоящее время. [42]
Теплота образования этих простейших веществ приведена в справочных таблицах. В этом веществе производится замена атомов водорода на группы СН3, необходимые для построения углеродного скелета химического соединения. Затем группы СН3 замещают на другие группы и в случае необходимости заменяют одинарные связи двойными или тройными связями. Тепловые поправки суммируются с теплотой образования основного вещества. Полученная сумма и есть искомая теплота образования вещества в газообразном состоянии. [43]
Страницы: 1 2 3