Аммонийный буфер
Cтраница 1
Аммонийный буфер представляет собой смесь гидроксида аммония и хлористого аммония. [1]
В отсутствие аммонийного буфера подщелачивание может проводиться гидроксидамк, карбонатами или гидрокарбонатами, в этом случае образуется буферная система карбонат / гидрокарбонат. [2]
Наиболее подходящим для этого разделения будет аммонийный буфер, так как железо ( III) аммиачных комплексов не образует, а устойчивость комплексов магния ( II) с аммиаком невелика и их образование даже улучшает разделение. [3]
К оттитрованной пробе добавляют 5 мл аммонийного буфера, а затем определяют остаточное содержание ионов щелочноземельных элементов по первому варианту комплексонометрического метода. [4]
Рассчитаем кривую титрования 100 0 мл 0 010 М Ni ( NOa) 2 в присутствии аммонийного буфера с рН 9 0 и концентрацией аммиака 0 2 моль / л раствором ЭДТА концентрации также 0 010 моль / л, считая, что объем раствора при титровании остается постоянным и равным 100 0 мл и ионная сила не меняется. [5]
Рассчитаем кривую титрования 100 0 мл 0 010 М № ( МОз) 2 в присутствии аммонийного буфера с рН 9 0 и концентрацией аммиака 0 2 моль / л раствором ЭДТА концентрации также 0 010 моль / л, считая, что объем раствора при титровании остается постоянным и равным 100 0 мл и ионная сила не меняется. [6]
Образуется белый кристаллический осадок смешанной кальций-аммонийной соли, нерастворимой в уксусной кислоте. Осаждение ведут в присутствии аммонийного буфера ( NH4OH NH4C1) при нагревании. [7]
По первому варианту к 0 2000 - 0 4000 г гидратированной смолы, отделенной от адгезионной воды центрифугированием [2], приливают 25 мл 20 % - ного раствора КС1, 5 мл аммонийного буфера ( содержащего 25 г / л NH3 и 20 г / л NH4C1) и 20 мл воды. Смесь выдерживают при периодическом взбалтывании 15 мин. [8]
Фиксированные группы монофункциональной иминодиуксусной смолы существуют в этом интервале значений рН в кислой форме ( ср. В таких щелочных условиях количественно адсорбируется и группа ионов Ni, Cd, Zn, Co. В интервале значений рН аммонийного буфера фиксированные группы смолы существуют в щелочной форме ( ср. [9]
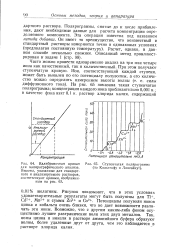 |
Калибровочная кривая для полярографического анализа. Высоты, указанные для стандартного и анализируемого растворов, соответствуют кривым, изображенным на 63. [10] |
Потенциалы полуволн ионов цинка и кобальта очень близки, что не дает возможности различать эти ионы. Возможно, что с другим каким-либо фоном осуществимо лучшее разграничение волн этих двух металлов. Так, ионы цинка и никеля в растворе аммонийного буфера образуют волны, более удаленные друг от друга, чем это наблюдается в растворе хлорида калия. [11]
По первому варианту к 0 2000 - 0 4000 г гидратированной смолы, отделенной от адгезионной воды центрифугированием [2], приливают 25 мл 20 % - ного раствора КС1, 5 мл аммонийного буфера ( содержащего 25 г / л NH3 и 20 г / л NH4C1) и 20 мл воды. Смесь выдерживают при периодическом взбалтывании 15 мин. Ионы Mg2 вытесняются в жидкую фазу медленнее Са2, потому Mg-форму катионита КУ-1 нужно дотитровывать комплек-соном III 2 - 3 раза. Во втором варианте комплексонометрического метода анализ начинают как и в предыдущем способе, но после добавления 20 % - ного КС1 к смеси приливают избыток стандартного раствора комплексона III и указанное количество аммонийного буфера, а затем оттитровывают непрореагировавший комплексообразователь ( после 30 мин. [12]
Страницы: 1