Пора - цеолит
Cтраница 3
Использованные органические растворители не способны проникать в систему пор цеолита А. Изотермы обмена описываются кривой с точкой перегиба, что связывают с протеканием двух различных ионообмен - ных процессов, обусловленных существованием в цеолите катион-вых центров двух типов. До степени обмена Liz 0 35 - 0 40 в обмене участвуют нелокализованные ионы а-полостей, при более высоких степенях обмена замещению подвергаются катионы, локализованные в местах S; на одинарных 6-членных кольцах. Относительная избирательность к литию уменьшается с ростом концентрации оранического растворителя. [31]
Третьим фактором является соответствие размеров реагирующих молекул с размерами пор цеолитов. Для протекания реакций необходимо, чтобы размер пор в цеолитах был больше критических размеров молекул реагирующих веществ и продуктов реакции ( см. табл. 4), поскольку эти реакции протекают в основном во внутрикристаллических полостях цеолитов. [32]
В этом разделе главы суммируются данные по определению объема пор цеолитов разного структурного типа ( по различным адсорбатам) и сравниваются экспериментальные и расчетные величины. [33]
Наряду с катионными активными центрами на поверхности или в порах цеолитов имеются ионы кислорода, а также поверхностные гидроксилыше группы; при этом ионы кислорода могут выступать как доноры. [34]
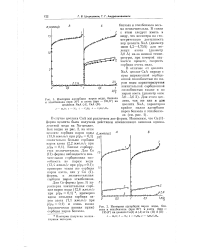
По данным [92] коэффициент кнудсеновской диффузии паров воды во вторичных порах цеолита NaA при t 20 С составляет 0 4 - 1 ( Г4 м2 / с, а коэффициент диффузии паров воды в азоте при той же температуре равен 0, 28 - КГ4 м2 / с. Подставив эти значения в соотношение ( 2 - 176), определим температуру Т 392 К, или / 119 С, при которой кинетические кривые десорбции паров воды из цеолита NaA в потоке и в вакууме практически должны совпадать. Можно полагать, что при более высоких температурах ( на рис. 2 - 47 при t 130 С) присутствие газа-носителя не снижает скорости десорбции паров воды по сравнению с высоковакуумной откачкой. [35]
Из изложенного выше следует, что простой и однозначной связи между размером пор цеолитов и их разделяющей способностью нет и что причиной изменения адсорбционных свойств цеолитов в этом случае является изменение химического состава. [37]
Большая внутренняя поверхность ( 400 - 800 м2 / г) и структура пор цеолитов определяют их особую пригодность в процессах разделения газов, а также для их глубокой осушки. По сравнению с аморфными алюмосиликатами цеолиты имеют более высокую термостабильность и легкую модифицируемость. [38]
Большая внутренняя поверхность ( 400 - 800 м2 / г) и структура пор цеолитов определяют их особую пригодность в качестве высокоселективных адсорбентов. По сравнению с аморфными алюмосиликатами цеолиты обладают обычно более высокой термостабильностью и легкой модифицируемостью, по которой они превосходят аморфные алюмосиликаты по кислотности поверхности. [39]
Нитрование протекает в каналах пор цеолита, причем пара-селективность реакции связана с размером пор цеолита. Нитрование толуола ускоряется за счет диссоциации HN03 с образованием нитроний-катиона и за счет активации и адсорбции толуола на катализаторе, поэтому его активность зависит не только от кислотных свойств, но и от гидрофобности катализатора. [40]
Выгорание остатков масла длится около 4 ч, затем начинается процесс удаления влаги из пор цеолитов. Выравнивание температур указывает, что поглощение тепла на испарение влаги прекратилось. Небольшой разброс температуры возможен за счет потерь тепла через стенки адсорбера. Разброс будет тем меньше, чем лучше выполнена тепловая изоляция адсорбера. [41]
В связи с этим следует иметь в виду, что несмотря на геометрическую доступность пор цеолита NaA ( диаметр окон 4 2 - 4 75А) для молекул азота ( диаметр 3 0 А) из-за низкой температуры, при которой изучается процесс, скорость сорбции очень мала. [43]
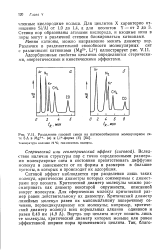 |
Разделение газовой смеси на катионообменном молекулярном сите 5 А в Mg2 - ( а и и - форме ( б. [44] |
Ситовой эффект наблюдается при разделении лишь таких молекул, критические диаметры которых соизмеримы с диаметрами пор цеолита. [45]
Страницы: 1 2 3 4