Новая порция - электролит
Cтраница 1
Новые порции электролита непрерывно подаются под колокол, а раствор щелочи, образовавшийся в результате электролиза, вытекает из верхней части сосуда. [1]
В нормально работающем электролизере электролит в межэлектродном промежутке движется вверх и с меньшей скоростью от анода к катоду. Новые порции электролита поступают снизу. Создается замкнутый поток электролита: в межэлектродном промежутке-вверх, затем из-под кромок диафрагм - в катодное пространство, в катодном пространстве электролит движется вниз. Благодаря большей площади сечения катодной ячейки электролит в ней движется с меньшей скоростью, позволяющей шарикам магния, вынесенным из межэлектродного пространства, всплыть на поверхность электролита. [2]
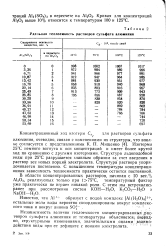 |
Удельная теплоемкость растворов сульфата алюминия. [3] |
Изотерма 25 С немного вогнута к оси концентраций и имеет более крутой ход по сравнению с другими изотермами. Структура льдоподобной воды при 25 С разрушается главным образом за счет введения в раствор все новых порций электролита. Структура раствора упорядочивается постепенно. С повышением температуры концентрационная зависимость теплоемкости практически остается постоянной. [4]
Электролит непрерывно с заданной скоростью циркулирует по замкнутому объему до достижения требуемой концентрации по активному хлору. Катодные отложения выносятся из электролизера, собираются в конусной части сепаратора, откуда периодически удаляются. Новая порция электролита добавляется в количестве, равном отведенному готовому продукту. [5]
Факт образования капиллярных протоков сам по себе очень примечателен. Он свидетельствует о наличии достаточно высоких градиентов давления в поровом пространстве, способных не только продвинуть влагу по капиллярам, но и сгладить стенки капилляров, деформировать бугорки, разрушая структуру грунта и формируя постоянные протоки. Таким образом, эффект раскачивания при импульсном воздействии способствует образованию в массиве оптимальных ( с гидравлической точки зрения) каналов, по которым отводится отработавший электролит, унося с собой продукты коррозии и уступая место новой порции электролита. [6]
Выше был рассмотрен случай электролиза на вращающемся дисковом электроде, помещенном в объем электролита. Вследствие трения слой электролита, непосредственно прилегающий к электроду, увлекается последним и под действием центробежной силы отбрасывается наружу в радиальном направлении от диска. Взамен отбрасываемого электролита к диску притекает в осевом направлении новая порция электролита и опять отбрасывается наружу. [7]
Анолит поело электролиза нейтрализуют содой или едким натром до слабощелочной реакции по фенолфталеину и упаривают до кашеобразного состояния или досуха. В первой порции дестиллята наряду с водой содержится неокисленный 3-пиколин. Спиртовый раствор никотината натрия отфильтровывают от осадка, который промывают на фильтре небольшим количеством спирта. После охлаждения суспензии отфильтровывают никотиновую кислоту, промывают на фильтре холодной водой и высушивают. Фильтрат и промывные воды присоединяют к новой порции нейтрализуемого электролита. Таким образом, потери никотиновой кислоты в процессе выделения практически отсутствуют. Новый метод выделения обладает рядом преимуществ: сокращается число операций и расход вспомогательных материалов, повышается чистота продукта, так как исключается применение солей меди и устраняется возможность попадания в продукт следов свинца; одновременно с выделением продукта регенерируется неокисленный 3-пиколин. [8]
 |
Схема обработки анодно-механическим методом. [9] |
Этот метод обработки поверхностей заготовки основан на использовании двух явлений: электроэрозии и электролиза. К электроэрозийной обработке его тяготит то, что тепловая энергия, возникшая из импульсных электрических разрядов в канале проводимости, производит направленное разрушение металла на обрабатываемой поверхности. А с электрохимической обработкой его сближает направленное растворение металла на аноде при превращении электрической энергии в химическую на границе заготовка-электролит и в самом электролите. В результате электролиза на поверхности анода образуется силикатная пленка, обладающая очень большим электрическим сопротивлением. Перемещающийся электрод-инструмент удаляет пленку и увлекает за собой новые порции электролита в прорезь. Так как электроды находятся под напряжением, процесс анодного растворения не прерывается. [10]
Этим методом получают медь, цинк, никель, кобальт, марганец, хром, железо, серебро, часть промышленного выпуска кадмия, олова, свинца, висмута, сурьмы и других металлов. Электролиз ведут как с нерастворимыми, так и с растворимыми анодами. При электролизе с нерастворимыми анодами на катоде осаждается чистый металл, а на аноде выделяется галоген или кислород и регенерируется соответствующая кислота. Например, при электролизе сернокислых растворов накапливается H2SC4 и в виде отработанного электролита возвращается в цикл для получения новых порций электролита. [11]
Серебро из него вытесняют ( цементируют) медью. Цементное серебро осаждается на дно. Обессеребренный раствор обычно выбрасывают. В некоторых же случаях его обезмеживают электролизом с нерастворимыми ( магнетитовыми) анодами. При этом содержание свободной азотной кислоты повышается примерно до 16 % и этот раствор может быть использован для приготовления новых порций электролита растворением в нем цементного серебра. [12]
Катодом служила платиновая проволока длиной 5 мм и толщиной 0.5 мм. При перенесении таким образом подготовленных анодов в новую порцию электролита постоянные значения напряжений разложения получаются после 20 - 30-минутного электролиза. [13]
Физической основой падения активности по сравнению с концентрацией является притягательное взаимодействие частиц. Взаимное отталкивание частиц в растворе должно, наоборот, вызывать увеличение активности. В разбавленных растворах электролитов электростатическое притяжение ионов оказывается преобладающим: v l и падает с ростом концентрации. Учет собственного размера ионов эквивалентен учету сил отталкивания, не позволяющих ионам сблизиться на расстояние, меньшее а. Второе приближение теории, учитывающее этот фактор, приводит к менее резкому уменьшению коэффициента активности ( рис. 10) и позволяет описать опытные данные в более широком интервале концентраций. Однако в концентрированных растворах большая часть молекул воды связана ионами, так что добавление новых порций электролита должно сопровождаться разрушением сольватных оболочек и преодолением сил ион - диполь-ного взаимодействия. [14]
 |
Зависимость среднего коэффициента активности от ионной силы в водном растворе NaCl. [15] |
Страницы: 1 2