Порядок - размещение - электрон
Cтраница 1
Порядок размещения электронов по молекулярным орбиталям тот же, что и в случае атомных орбиталей: прежде всего заполняются орбитали с низкой энергией; заполнение орбиталей подчиняется принципу Паули ( на каждой орбитали может быть не более двух электронов с противоположными спинами) и правилу Хунда. [1]
Такой порядок размещения электронов в атоме углерода представляет собой частный случай общей закономерности, выражаемой прав и л ом Хунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. [2]
Такой порядок размещения электронов в атоме углерода представляет собой частный случай общей закономерности, выражаемой правилом Хунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. [3]
Такой порядок размещения электронов в атоме углерода представляет собой новый пример из общей закономерности, выражаемой правилом Хунда. [4]
Такой порядок размещения электронов в атоме углерода представляет собой частный случай общей закономерности, выражаемой правилом Хунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. [5]
Такой порядок размещения электронов в атоме углерода представляет собой частный случай общей закономерности, выражаемой правилом Хунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома - максимально. [6]
Такой порядок размещения электронов в атоме углерода представляет собой частный случай общей закономерности, выражаемой правилом Хунда: устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня, при котором абсолютное значение суммарного спина атома максимально. [7]
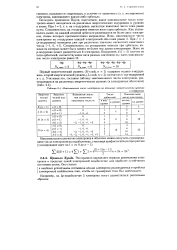 |
Максимальное число электронов на атомных энергетических уровнях. [8] |
Это правило определяет порядок размещения электронов в пределах одной электронной подоболочки для наиболее устойчивого состояния атома. [9]
Должна ли периодическая система элементов, отображающая закон развития материи, отображать фактический порядок размещения электронов в электронной оболочке. И она действительно отображает строение атома любого элемента. К сожалению, преподаватели химии этого, как правило, не подозревают. А между тем в показе того, как можно при помощи периодической системы расшифровать строение любого атома ( и оболочки, и ядра), состоит одна из важнейших задач изучения химии, одно из важнейших доказательств того, что периодическая система - естественная система. [10]
Должна ли периодическая система элементов, отображающая закон развития материи, отображать фактический порядок размещения электронов в электронной оболочке. И она действительно отображает строение атома любого элемента. К сожалению, преподаватели химии этого, как правило, ив подозревают. А между тем в показе того, как можно при помощи периодической системы расшифровать строение любого атома ( и оболочки, и ядра), состоит одна из важнейших задач изучения химии, одно из важнейших доказательств того, что периодическая система - естественная система. [11]
Страницы: 1