Порядок - расположение - орбиталь
Cтраница 1
Порядок расположения орбиталей для плоской молекулы H2XY показан на фиг. [1]
Порядок расположения орбиталей по энергии и корреляция орбиталей для линейной молекулы XY2 были уже рассмотрены ранее в связи с обсуждением результатов, представленных на фиг. [2]
Порядок расположения орбиталей по энергии для плоской формы молекулы С2Н4 и их корреляция с орбита-лями СН2 были показаны ранее на фиг. Связывающая орбиталь не имеет узловой плоскости, а разрыхляющая орбиталь имеет узловую плоскость, проходящую между двумя атомами углерода. Следовательно, суммарное связывающее действие этих четырех орбиталей будет мало. Этот факт находит отражение на фиг. [3]
Порядок расположения орбиталей по энергии слева и справа из теоретических соображений определяется неоднозначно. На диаграмме не приведены ls - орбитали атомов X и Y, однако они учтены при нумерации орбиталей. [4]
Аналогичным образом можно установить порядок расположения орбиталей, показанный на фиг. [5]
Для плоских молекул ХН3 порядок расположения орбиталей показан на фиг. [6]
Так может быть установлен порядок расположения орбиталей молекулы С6 в колонке слева от центра на фиг. Если теперь принять во внимание орбитали, получающиеся из 1 н-орбиталей, то необходимо будет провести дальнейшую перегруппировку орбиталей типа aig, elu, e2g и biu, как это показано в центре фиг. SH) сдвигается вверх из-за взаимодействия с орбиталью blu ( 2sc), которая расположена сравнительно высоко. Поскольку типы симметрии молекулярных орбиталей, получающихся из 2р2 - орбита-лей, не встречаются у других орбиталей, то эти орбитали остаются без изменения при такой перегруппировке. [7]
Эти состояния получены вышеописанным способом в предположении, что порядок расположения орбиталей тот же, что и ранее на фиг. В этой таблице обозначение ( l i) 2 относится к АГ-оболочке атома X. Оно не повторяется в последней колонке. Большинство из состояний, предсказываемых согласно табл. 33, наблюдалось экспериментально. [8]
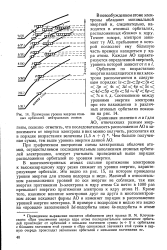 |
Примерные уровни энергии атомных орбиталей нейтральных атомов. [9] |
При графическом построении схемы электронных оболочек атомов, осуществляемом последовательным заполнением атомных орбита-лей электронами, следует учитывать приведенный выше порядок расположения орбиталей по уровням энергии. [10]
Эффект заметен в случае плоского силана SiH4, в котором пустые rf - орбитали кремния еще лежат достаточно высоко и эффективно не участвуют в связывании, но порядок расположения орбиталей ниой, чем у плоского метана. [11]
Такое расположение МО по энергии наблюдается для всех гомоядерных двухатомных молекул, образованных элементами второго периода, кроме 02 и F2; в этих же молекулах орбитали яи2р и og2p заполнены, и поэтому расположение их по энергии оказывается существенным лишь при рассмотрении возбужденных состояний. Однако если не рассматривать возбужденные состояния, то порядок расположения орбиталей по энергиям [ выражение (10.25) ] позволяет объяснить свойства симметрии основного состояния всех гомоядерных двухатомных молекул, образованных элементами второго периода, и их положительных ионов столь же успешно, как это удается сделать при выявлении свойств симметрии основных состояний элементов на основе расположения по энергиям АО ( гл. В табл. 10.2 приведены электронные конфигурации, соответствующие основному состоянию гомоядерных двухатомных молекул от Н2 до F2 и некоторых положительных молекулярных ионов. [12]
 |
Энергии электронных уровней в ато-1 - ме водорода. [13] |
Для многоэлектронных атомов приходится пользоваться приближенными решениями уравнения Шредин-гера. Существует правило, сформулированное В. М. Клеч-ковским, которое отражает порядок электронных состояний ( орбиталей) по энергии. Порядок расположения орбиталей по энергиям, изображенный на рис. 10, справедлив только для легких элементов. Начиная с цинка, вследствие все более высокого положительного заряда ядер, картина осложняется, о чем несколько подробнее будет сказано далее. [14]
Для многоэлектронных атомов приходится пользоваться приближенными решениями уравнения Шредин-гера. Существует правило, сформулированное В. М. Клеч-ковским, которое отражает порядок: электронных состояний ( орбиталей) по энергии. Порядок расположения орбиталей по энергиям, изображенный на рис. 10, спра ведлив только для легких элементов. Начиная с цинка, вследствие все более высокого положительного заряда ядер, картина осложняется, о чем несколько подробнее будет сказано далее. [15]
Страницы: 1 2