Порядок - реакция - инициирование
Cтраница 1
Порядок реакции инициирования ( а также значения s) указан на кривых. Сплошные и пунктирные кривые относятся к обрыву диспропорционированием и соединением радикалов соответственно. [1]
Из уравнений ( 7) - ( 9) видно, что порядок реакции инициирования по мономеру может быть любым - от нулевого до второго, в зависимости от состояния равновесий ( 1) или ( 5) и механизма превращения X в активный центр. Корректные кинетические данные в этой области, однако, отсутствуют. [2]
Из уравнений ( 7) - ( 9) видно, что порядок реакции инициирования по мономеру может быть любым - от нулевого до второго, в зависимости от состояния равновесий ( 1) или ( 5) и механизма превращения X в активный центр. Корректные кинетические данные в этой области, однако, отсутствуют. [3]
Чтобы приписать какой-то реакции определенный механизм, следует учесть целый ряд факторов. Так, например, порядок реакции инициирования зависит от сложности диссоциирующей молекулы, температуры эксперимента и давления. [4]
Оценку этих данных затрудняет то обстоятельство, что порядок реакции инициирования до сих пор не был определен достаточно надежно. Согласно исследованиям Майо [134], Хиатта и Барт-летта [135], реакция инициирования является тримо-лекулярной реакцией, а согласно более новым исследованиям Кирхнера [120], она бимолекулярна. Более ранние исследования Майо относительно передачи цепи ( см., например, работу [136]) были согласованы также с бимолекулярным механизмом. Рассмотрение этой проблемы с помощью гипотезы горячих радикалов опять-таки скорее подтверждает бимолекулярный механизм. [5]
Уравнения ( V-15) и ( V-19) не исчерпывают всех возможных случаев зависимости скорости полимеризации от концентрации мономера и возбудителя в катионных системах. Как будет показано далее, природа реагирующих веществ и растворителя способна влиять на порядок реакции инициирования и приводить к соответствующим изменениям в уравнениях общей скорости процесса. Кроме того, сама правомерность применения принципа квазистационарности к процессам катионной полимеризации далеко не всегда очевидна. [6]
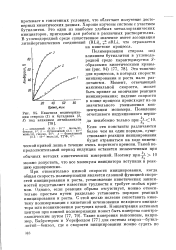 |
Кинетика полимеризации стирола ( 1 и бутадиена ( 2, 3 под влиянием литийалкилов. [7] |
При относительно низкой скорости инициирования, когда общая скорость полимеризации является сложной функцией скоростей инициирования и роста, установление кинетических зависимостей представляет известные трудности и требует особых приемов. Однако, если реакция обрыва отсутствует, можно относительно простым путем раздельно установить порядок реакций инициирования и роста. С этой целью полезно сопоставить кинетику полимеризации с кинетикой исчезновения исходного инициатора или возникновения растущих цепей. [8]
Уравнения ( V-15) и ( V-19) не исчерпывают всех возможных случаев зависимости скорости полимеризации от концентрации мономера и возбудителя в катионных системах. Как будет показано далее, природа реагирующих веществ и растворителя способна влиять на порядок реакции инициирования и приводить к соответствующим изменениям в уравнениях общей скорости процесса. Кроме того, сама правомерность применения принципа квазистационарности к процессам катионной полимеризации далеко не всегда очевидна. [9]
При относительно низкой скорости инициирования, когда общая скорость полимеризации является сложной функцией скоростей инициирования и роста, установление кинетических зависимостей представляет известные трудности и требует особых приемов. Однако, если реакция обрыва отсутствует, можно относительно простым путем раздельно установить порядок реакций инициирования и роста. С этой целью полезно сопоставить кинетику полимеризации с кинетикой исчезновения исходного инициатора или возникновения растущих цепей. [10]
Подобным образом, если принять, что инициирование цепи происходит как бимолекулярная реакция, то вся реакция в целом также была бы второго порядка. Все кинетические данные, полученные для различных типов механизмов реакций, были обработаны Голъдфинге-ром, Летортом и Никлозом [12], составившими на основании этих данных таблицу, по которой может быть определен порядок реакции в целом, если известен порядок реакций инициирования и обрыва цепи. [11]
Значения k м рассчитанные в ранних работах по результатам опытов со стиролом в растворе, отличаются от соответствующих значений, полученных при полимеризации чистого стирола, низким значением численного множителя. Учитывая особенности этой реакции, уже рассмотренные на стр. По мнению Майо [10], третий порядок реакции инициирования находится в хорошем соответствии с полученными экспериментальными данными для широкого интервала концентраций стирола. [12]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимора. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-номера реакция может остановиться полностью. [13]
Дальнейшая судьба окклюдированных радикалов зависит от физич. В среде осадителя растущие радикалы сворачиваются в достаточно плотные клубки, и активный конец радикала оказывается спрятанным внутри клубка. Кроме того, клубки коагулируют, образуя осадок полимерной фазы. Это приводит к увеличению как средней концентрации радикалов в системе, так и в особенности их концентрации в частицах полимера. Обрыв цепи происходит либо в результате взаимодействия застрявших радикалов с более подвижными радикалами, приходящими из объема жидкой фазы, либо в результате полного захоронения застрявших радикалов в массе полимера. Наблюдаемое часто повышение порядка реакции инициирования по сравнению с гомогенной полимеризацией в жидкой фазе указывает на преобладание второго механизма. Скорость роста цепи с участием окклюдированных радикалов также несколько замедляется вследствие замедленной диффузии мономера внутрь полимерных клубков. Но этот эффект, как правило, перекрывается значительно большим снижением скорости обрыва цепей. Поэтому общая скорость реакции при переходе от гомофазной к гетерофазной полимеризации обычно возрастает. При очень малых скоростях диффузии мо-иомера реакция может остановиться полностью. [14]
Страницы: 1