Порядок - электрохимическая реакция
Cтраница 1
Порядок электрохимической реакции имеет тот же смысл, что и в учении о кинетике химических реакций. Этот метод применим в тех случаях, когда система достаточно удалена от состояния равновесия. [1]
Использование порядка электрохимической реакции для решения одной из основных задач электрохимической кинетики - установления пути, по которому протекает данная реакция - можно проиллюстрировать на примере восстановления иода до иодид-ио-нов. [2]
Использование порядка электрохимической реакции для решения одной из основных задач электрохимической кинетики - - установления пути, по которому протекает данная реакция, - можно проиллюстрировать на примере восстановления иода до иодид-ионов. [3]
Использование порядка электрохимической реакции для решения одной из основных задач электрохимической кинетики - установления пути, по которому протекает данная реакция, - можно проиллюстрировать на примере восстановления иода до иодид-ио-нов. [4]
Показатели сте-ени zT и ZD указывают на порядок электрохимической реакции и имеют такое же значение для установления механизма электрохимической реакции ( перехода электрона), как порядок химической реакции для выяснения ее механизма. Как будет показано ниже, в большинстве случаев порядок электрохимической реакции равен единице. [5]
Ответив на предыдущий вопрос, подумайте, как найти порядок электрохимической реакции относительно вещества, принимающего участие в реакции перехода электрона. [6]
Здесь величины zBtj и z0j, согласно Феттеру, характеризуют порядок электрохимической реакции по соответствующему компоненту. По смыслу эта величина вполне аналогична порядку химической реакции. [7]
Как следует из приведенных уравнений, порядок каталитической реакции по ионам металла и восстановителю отличается от порядка соответствующих электрохимических реакций - вместо первого он равен аи 1-а. Так как а обычно меньше 1, то и порядок каталитической реакции будет ниже первого, что соответствует экспериментальным данным. [8]
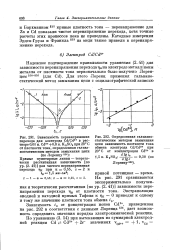
Зависимость г0 от концентрации ионов Gd2, приведенная на рис. 292 в соответствии с данными Лоренца ш, дает возможность определить значения порядка электрохимической реакции. [10]
Двумя другими важными характеристиками электрохимических реакций являются их порядок и стехиометрическое число. Порядок электрохимической реакции v имеет здесь тот же физический смысл, что и в учении о кинетике химических реакций, хотя в этом случае v, кроме обычных параметров - давления и температуры, может быть функцией потенциала электрода. [11]
Показатели сте-ени zT и ZD указывают на порядок электрохимической реакции и имеют такое же значение для установления механизма электрохимической реакции ( перехода электрона), как порядок химической реакции для выяснения ее механизма. Как будет показано ниже, в большинстве случаев порядок электрохимической реакции равен единице. [12]
Страницы: 1