Порядок - стабильность
Cтраница 1
Порядок стабильностей для комплексов Ag ( l) и, вероятно, кадмия с замещенными бензолсульфонатами следующий: фосфор мышьяк азот. Комплексы кадмия гораздо менее стабильны, чем комплексы Ag ( I), и отличие в устойчивости между комплексами с фосфинами и аминами значительно меньше. [1]
Порядок стабильности 2 4: 3 5-ди - О-метиленпроиз-водных с манно -, глюко - и wdo - конфигурациями наглядно демонстрируется тем фактом [139] что 2 4: 3 5-ди - О-метилен-в - гексосахарные кислоты с манно - и глю / со-конфигурациями легко эпимеризуются при катализе основаниями в 2 4: 3 5-ди - О-метилен-ь - идоса-харную кислоту. [2]
Этот порядок стабильности отражает отношение углеводородов к термическому разложению и взаимодействию с химическими реагентами, включая кислород. Термическая устойчивость ненасыщенных углеводородов относительно насыщенных зависит от температуры. [3]
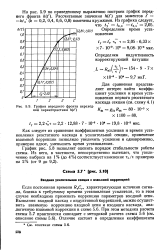 |
График переднего фронта переходной характеристики h ( t. [4] |
График рис. 5.8 позволяет оценить порядок стабильности работы схемы. [5]
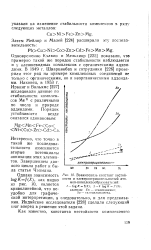 |
Взаимосвязь констант нестой. [6] |
Одновременно Кэлвин и Мельхиор [225] показали, что примерно такой же порядок стабильности наблюдается и у клешневидных комплексов с органическими адден-дами. [7]
Интересно отметить, что исследование стабильности подобных соединений с N-метилзамещенными циклическими имина-ми [335] дает обратный по сравнению с незамещенными имина-ми порядок стабильности 3 4 5 6, хотя порядок основности их сохраняется. Этот эффект можно объяснить пространст-менными затруднениями, которые возрастают с ростом величины цикла и приводят к систематическому снижению стабильности продуктов присоединения. Он свидетельствует о решающем влиянии пространственного фактора на стабилизацию координационных соединений с объемистым триметилбором. [8]
Было найдено, что в газовой фазе устойчивым является протонированиьтй по ребру циклопропан. Однако авторы отмечают, что в растворах порядок стабильности существенно меняется вследствие большей энергии сольватации 2 - и I-пропильных катионов по сравнение с протонированными формами циклопропана и, таким образом, эти данные не противоречат экспериментально установленной большей стабильности 2-пропильного катиона в конденсированных фазах. [9]
В) действительно соответствует второй по стабильности рассчитанной форме. Поскольку разность энергий между первой и второй стабильными формами невелика, порядок стабильности может быть легко обращен благодаря присутствию заместителей или же энергии решетки кристалла. [10]
В циклогексанонах эти формы обычно возникают в связи с тем, что при переходе к форме ванны уменьшается сильное 1 3-диаксиальное отталкивание. Имеется однако ряд случаев, которые пока еще остаются неясными. Зонхеймер и сотрудники [194] показали, что хотя 2а - метилхолестанон-3 более стабилен, чем соответствующий 2р - эпимер, при введении двойной связи в положение 6 порядок стабильности оказывается обратным. Большая стабильность 2р - эпимера находится в соответствии с формой ванны. Стабильность формы ванны в этих системах, однако, не была как-либо объяснена. [11]
Уменьшение напряжения кольца в пяти - и шестичленных циклах делает это влияние менее существенным. Однако в циклических гидразинах ограничение внутримолекулярной релаксации, вызванное взаимозависимостью связанных кольцом групп, делает влияние стерических факторов более заметным чем в алкилгид-разинах. По данным ФЭС, производные пиразолидина ( табл. 6) могут находиться в двух конформациях, хотя обе наблюдаются только в минимально стериче-ски затрудненных пиразолидине и 1 2-диметилпиразолидине, причем если для пиразолидина более устойчивой является конформация с меньшим торсионным углом между неподеленными парами, то для 1 2-диметилпиразолидина порядок стабильности обратный. [12]
Переход от газовой фазы к конденсированной способствует стабилизации гош-конформера. Увеличение объема заместителей при связи С - С приводит к усилению гош-отталкивания. Для гомологов бутана порядок стабильности аналогичен. [13]
Это было определено в отсутствие газа-переносчика путем наблюдения вышеописанным образом скорости исчезновения теллурового зеркала. Предполагая мономолекулярную реакцию, полупериод жизни был найден равным 6 10 - 8 сек. В холодной трубке продолжительность жизни бензильного радикала значительно меньше, чем метильного, возможно благодаря большому коэфициенту аккомодации трубки для первого. Однако при высоких температурах оба радикала достигают одного порядка стабильности. [14]
Страницы: 1