Эффективный порядок - реакция
Cтраница 1
Здесь эффективный порядок реакции меняется от второго до нулевого. Если медленной стадией является адсорбция, то кинетика остается такой же, как и для мономолекулярной реакции. [1]
Таким образом, эффективный порядок реакции распада гидразина по гидразину составляет от пэ I для низких давлений до гаэ 1 5 для высоких давлений. [2]
Полученные в двух рассмотренных примерах величины Ев и эффективного порядка реакции / гэф 2 дают основание определить детонацию. [3]
Полученные в двух рассмотренных примерах величины E3 и эффективного порядка реакции лэф 2 дают основание определить детонацию как высокотемпературное цепочечно-тепловое воспламенение, лимитируемое зарождением активных центров. [4]
Таким образом, влияние такого выбора концентрации состоит в уменьшении эффективного порядка реакции. [5]
Уже на этом простейшем примере виднй важнейшая особенность гетерогенных реакций: эффективный порядок реакции может быть меньше единицы. Для реакций на однородной поверхности этот эффективный порядок меняется с концентрацией. В случае неоднородной поверхности, как мы увидим ниже, реакция может в широком интервале концентраций иметь постоянный дробный порядок. В процессах гетерогенного катализа гораздо чаще встречается противоположный случай, когда скорость процесса определяется медленной активированной адсорбцией. [6]
Уже на этом простейшем примере вицна важнейшая особенность гетерогенных реакций: эффективный порядок реакции может быть меньше единицы. Для реакций на однородной поверхности этот эффективный порядок меняется с концентрацией. В случае неоднородной поверхности, как мы увидим ниже, реакция может в широком интервале концентраций иметь постоянный дробный порядок. В процессах гетерогенного катализа гораздо чаще встречается противоположный случай, когда скорость процесса определяется медленной активированной адсорбцией. [7]
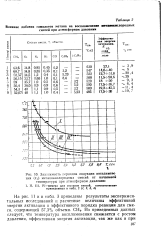 |
Зав. симость периодов индукции воспламенения ( т / метанокислородных смесей от начальной температуры при атмосферном давлении. [8] |
На рис. 11 и в табл. 3 приведены результаты экспериментальных исследований и расчетные величины эффективной энергии активации и эффективного порядка реакции для смеси, содержащей 57 3 % объемн. [9]
ДЯ - величина, постоянная для данной химической реакции, равная произведению константы скорости реакции, теплового эффекта реакции и п - е 1 - величины эффективного порядка реакции. [10]
На анализе термограмм основаны количественные методы термографии - определение термодинамических и кинетических характеристик химических процессов и фазовых переходов: теплового эффекта, мощности внутренних источников теплоты, констант скоростей эффективного порядка реакции и пр. [11]
После того как расчетом ( с использованием ЭВМ) была подтверждена возможность зависимости W cf, где Wt - скорость синтеза НС1О4, с1 - концентрация С12 и п - эффективный порядок реакции, превышающий единицу в интервале изменения концентраций С12 на несколько порядков [97], была поставлена обратная задача - рассчитать по данным кинетических экспериментов константы скоростей элементарных реакций, обеспечивающие наилучшее согласие расчета с опытом в различных условиях. [12]
 |
Влияние давления окиси. [13] |
Па эффективная удельная скорость реакции заметно возрастает. Суммарный эффективный порядок реакции карбидирования железа по окиси углерода близок к нулю ( - 0 1), а в интервале давлений окиси углерода 3 3 - 104 - f - 3 - 105 Па равен нулю с высокой точностью. В связи с этим можно полагать, что стационарная концентрация хемосорби-рованной на поверхности железа окиси углерода или образовавшихся на ее основе промежуточных комплексов близка к макси-ную скорость реакции карбидиро - МаЛЬНО ВОЗМОЖНОЙ. [14]
Он пришел к выводу, что характер поверхности, на которой протекает реакция, играет большую роль в механизме полимеризации. Поэтому было трудно определить эффективный порядок реакции и другие кинетические константы, так как отсутствовала воспроизводимость результатов. [15]
Страницы: 1 2