Частный порядок
Cтраница 2
Если концентрации исходных веществ различны, то для выделения частного порядка реакции по одному из компонентов VA, VB... [16]
Наиболее последователен вариант I, так как он не изменяет также частного порядка взаимного расположения символов химических элементов и числовых индексов при них. [17]
Наиболее последователен вариант I, так как он не изменяет также частного порядка взаимного расположения символов химических элементов и числовых индексов при них. В соответствии с этим вариантом находится усиливающаяся ( главным образом, под влиянием быстро растущего многообразия веществ) тенденция к широкому использованию не словесных названий неорганических соединений, а непосред. [18]
Если в реакции участвуют несколько веществ и уравнение имеет вид (1.9), то частный порядок реакции по каждому из веществ можно найти следующим образом: берут все вещества, кроме одного, в столь большом избытке, что относительным изменением их концентраций можно пренебречь. Тогда кинетическое уравнение приобретает вид W k C. [19]
Де Вожелер [ неопубликовано ] поочередно использовал два различных релаксационных множителя о и со для некоторого частного порядка. Это не привело к значительному улучшению результатов на практике, но с теоретической точки зрения представляет интерес. [20]
 |
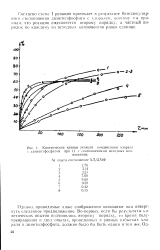
Кинетические кривые реакции конденсации хлораля с диметнлфосфитом при 11 с соотношениями исходных компонентов. [21] |
Согласно схеме I реакция протекает в результате бимолекулярного столкновения диметилфосфита с хлоралем, поэтому мы приняли, что реакция подчиняется второму порядку, а частный порядок по каждому из исходных компонентов равен единице. [22]
 |
Кинетические кривые реакции конденсации хлораля с диметилфосфитом при И с соотношениями исходных компонентов. [23] |
Согласно схеме I реакция протекает в результате бимолекулярного столкновения диметилфосфита с хлоралем, поэтому мы припили, что реакция подчиняется второму порядку, а частный порядок по каждому из исходных компонентов равен единице. [24]
Для этого проводят реакцию в условиях практического постоянства ( обычно при значительном избытке) всех компонентов, кроме одного, определяют одним из методов частный порядок по этому компоненту. Повторив эту операцию для каждого компонента, находят все частные порядки и получают в явном виде кинетическое уравнение реакции. [25]
Мутация может привести как к ароморфозу ( арогенезу) - резкому расширению сферы обитания вида, возникновению многих близких форм, так и к аллогенезу ( идиоадаптаций) - изменениям частного порядка. [26]
Таким образом, в первую очередь реакцию рассматривают как отвечающую определенному порядку; если оказывается, что это не так, то следует, например, путем упрощения ( вырождения) выявить сначала такие исходные вещества, по которым частный порядок вполне определенный. На основании влияния на фиктивную константу других реагентов определяют функцию, отражающую их влияние на скорость. [27]
Различают частный и общий порядок реакции. Частный порядок определяется по изменению концентрации одного из реагирующих веществ. Сумма частных порядков дает общий порядок реакции. Частный порядок находится несколькими методами. [28]
Сумма показателей степеней концентраций реагентов в кинетическом уравнении реакции называется порядком химической реакции. Порядок по данному веществу ( частный порядок) определяется как показатель степени при концентрации этого вещества. [29]
И по этим вопросам и по вопросам частного порядка необходимо обеспечить возможность широкой дискуссии в печати, на всякого рода собраниях, совещаниях в центре и на местах. Решать же их придется, вероятно, в коллегиях с более узким составом. [30]
Страницы: 1 2 3 4